Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Absorption (Physik)Der Begriff Absorption (lat.: absorptio = Aufsaugung) bezeichnet im Allgemeinen das Aufsaugen, das In-sich-Aufnehmen von etwas. Die Stärke der Absorption wird bei Teilchenströmen und Wellen durch einen Materialparameter beschrieben, den Absorptionsgrad α, engl. absorption coefficient, der i. d. R. von einer Vielzahl von Parametern (Temperatur, Wellenlänge) abhängig ist und bei großen Feldstärken nichtlinear werden kann. Weiteres empfehlenswertes Fachwissen
Absorption von Wellen und TeilchenstrahlenBei der Absorption von Wellen in einem absorbierenden, homogenen Material, ist die Wahrscheinlichkeit der Absorption pro Wegeinheit in jeder Eindringtiefe gleich. Dann gilt ein exponentielles Gesetz, das Bouguer-Lambertsche Gesetz (oft kurz Lambertsches Gesetz genannt, vergleiche aber Lambertsches Kosinusgesetz). Ist I0 der ursprüngliche Strom, beträgt der nach Durchlaufen der Schichtdicke d noch vorhandene Strom I(d): (Herleitung des Gesetzes: siehe Absorptionsgesetz). Dabei ist μ der von den Eigenschaften des absorbierenden Materials und oft auch von der Energie (Quantenenergie, Teilchenart und -geschwindigkeit) der Strahlung abhängige Absorptionskoeffizient. Sein Kehrwert ist die Eindringtiefe. Aus ihm lässt sich die Dicke der Halbwertsschicht berechnen. SchallDie Absorption von Schall findet durch Umwandlung der Leistung des Schalles (Luftschall, Körperschall, auch Erdbebenwellen) in thermische Energie in einem dämpfenden Medium oder an Grenzschichten (z. B. zwischen Luft, in der sich der Schall ausbreitet und einer Festkörperoberfläche) statt (Näheres siehe Schalldämpfung). Die Schallabsorption in Luft ist durch verschiedene thermodynamische Vorgänge bedingt. Elektromagnetische WellenLichtAbsorbierte Lichtanteile werden nicht nur zu Wärme, sondern können auch durch Streuung an Aerosolen oder z. B. durch Fluoreszenz verloren gehen. Die Menge der auf dem Weg nicht absorbierten oder gestreuten Photonen hängt dabei nach dem Lambert-Beerschen Gesetz von der Schichtdicke des Materials ab. Daher ist z. B. der Himmel im Gebirge dunkler und die Sonne heller. Siehe auch: Absorptionsbande, Absorptionswerte chemischer Substanzen, Extinktion(optische Dichte (ND) = Absorbanz), Lichtleitkabel Röntgen- und GammastrahlungAuch beim Durchgang von Röntgen- und Gammastrahlung durch Materie ist die Wahrscheinlichkeit für Absorption der Dicke d des durchstrahlten Stoffes proportional. Daraus ergibt sich eine exponentielle Abnahme der Intensität mit der Dicke: Hier ist μ = n · σ der Absorptionskoeffizient, gemessen in m−1, n die Zahl der Atome im Material pro m3 und σ der Wirkungsquerschnitt für Absorption. In der Optik (siehe oben) heißt dieses Gesetz das Lambertsche Gesetz. Man kann die Schwächung des Strahls auch durch eine Halbwertsdicke beschreiben; diese ist dem Absorptionskoeffizienten umgekehrt proportional. Ein Gammaquant kann folgendermaßen absorbiert werden:
Die Wahrscheinlichkeit bzw. der Wirkungsquerschnitt für jeden dieser Prozesse hängt von der Energie der Photonen und der Ordnungszahl der Materie ab: der photoelektrische Effekt überwiegt für kleine Energien und hohe Ordnungszahl, die Paarbildung für hohe Energien und hohe Ordnungszahl, der Comptoneffekt für mittlere Energien und niedrige Ordnungszahl. Der Gesamt-Wirkungsquerschnitt für Absorption ist gleich der Summe aus den Einzelquerschnitten für die drei Prozesse:
Die freigesetzten Elektronen aus allen drei Prozessen können ihrerseits bei genügender Energie weiter ionisierend wirken. Die beschriebene exponentielle Abnahme gilt nur im Idealfall bei einem dünnen Strahl ohne Hineinstreuung von außen; sie gilt nicht für die Absorption durch eine breite Betonwand. FernerkundungIn der Fernerkundung bezieht sich der Ausdruck Absorption auf das Aufnehmen von elektromagnetischer Strahlungsenergie durch die Atmosphäre oder die Erdoberfläche. So wird vorübergehend Energie gespeichert und entsprechend dem Planckschen Strahlungsgesetz wieder emittiert. So reemittiert die durch die Sonne erwärmte Erdoberfläche Strahlung im Wellenlängenbereich des mittleren Infrarot (etwa 8 bis 14 µm). Diese Strahlung wird durch Wolken oder Treibhausgase absorbiert und so verzögert in den Weltraum bzw. wieder zur Erde reemittiert. Daher wird es in klaren Nächten kälter als in bedeckten. LIDAR ist in der Lage, ein Schichtprofil der Konzentration von Spurengasen zu liefern. Hierbei wird mit speziellen Wellenlängen gearbeitet, die die Moleküle der Spurengase selektiv anregen und so absorbiert und reemittiert werden. Auch ein Profil der Windgeschwindigkeit kann gewonnen werden (Dopplerverschiebung rückgestreuter Strahlung). Farb- bzw. wellenlängenabhängige Absorption der Erdoberfläche hilft, zwischen verschiedenen Bedeckungen zu unterscheiden. Man nutzt den sichtbaren und den infraroten Spektralbereich, um Vegetationsarten und Temperaturen zu bestimmen. Mit satellitengestütztem Radar kann man Oberflächenprofile gewinnen, aber auch Wellenfrequenz und -höhe bestimmen. FunkwellenFunkwellen zur Nachrichtenübertragung oder beim Radar werden in der Atmosphäre durch freie Ladungsträger (Ionisierung) sowie Regen und Schnee bzw. Hagel absorbiert, reflektiert und gestreut. Bei Sonnenstürmen kann es zum Erliegen des Funkverkehrs kommen, wenn die Atmosphäre bis in niedrige Schichten ionisiert wird und Funkwellen absorbiert. Absorption in der VerfahrenstechnikAbsorption von StoffenDie Absorption eines Stoffes durch einen anderen meint eine Vermischung ohne chemische Reaktion. Der Vorgang der Absorption wird durch eine Affinität des einen Stoffes für den anderen hervorgerufen - es besteht eine bestimmte Löslichkeit der Stoffe ineinander. Handelt es sich um ein geschlossenes System z. B. mit einer Flüssigkeit und einem Gas, so 'strömen' zunächst Atome oder Moleküle in die Flüssigkeit, bis die Löslichkeit des Gases in der Flüssigkeit erreicht ist. Dabei handelt es sich dann um ein dynamisches Gleichgewicht, d. h. der Teilchenstrom in die Flüssigkeit ist genauso groß wie der Teilchenstrom in die Gasphase. Die Absorptionsrate wobei L die Löslichkeit ist (hier als absolute Menge). Die Absorption von Gasen kann nicht nur in eine Flüssigkeit sondern auch in einen festen Stoff erfolgen. Dieser wird Absorptionsmittel (oder Absorbens), das aufgenommene Gas wird Absorbat genannt. Das Gas wird bei gegebener Temperatur im Absorptionsmittel gelöst, wobei Wärme (Absorptionswärme oder Lösungswärme) entsteht. Finden bei der Lösung der Gase keine chemischen Reaktionen statt, so gilt für Flüssigkeiten bei niedrigem Druck näherungsweise das Henrysche Gesetz:
Hierbei ist k der Absorptionskoeffizient, der von der Temperatur und den beteiligten Stoffen abhängt. Sind mehrere Gase an der Absorption beteiligt, so werden sie unabhängig voneinander gemäß ihrem jeweiligen Partialdruck px in der Gasphase gelöst:
Sind bei einem Gas mehrere nicht mischbare Flüssigkeiten als Absorptionsmittel beteiligt, so ist das Verhältnis der Konzentrationen unabhängig von der Menge des gelösten Stoffes und der Flüssigkeiten und hängt nur von der Temperatur und den Stoffen ab; siehe Nernstscher Verteilungssatz. Die Absorption von Gasen in Flüssigkeiten wird in der Kältetechnik für Absorptionskältemaschinen verwendet. Absorption / AdsorptionSchwebstoffe werden durch Filter aus einem Flüssigkeits- oder Gasstrom gefiltert. Werden dagegen Flüssigkeits- oder Gasbestandteile durch eine reaktive Oberfläche (Aktivkohle, Zeolithe) fest gebunden, so spricht man von Adsorption. Das Maß der Filtration hängt hier von der Rückhaltefähigkeit und Aufnahmefähigkeit ab. Bei mechanischen Filter steigt die Rückhaltefähigkeit mit der Belegung, da die Schwebstoffe langsam die feinen Poren des Filters zusetzen. Dabei nimmt auch der Luftwiderstand des Filters zu und dessen Porengröße ab. Wird ein Gas- oder Luftstrom durch eine Waschflüssigkeit geleitet, so spricht man von Gaswäsche oder auch von Absorption. Dabei werden die zu absorbierenden Gaskomponenten (Absorptiv - ungebunden, Absorbt - gebunden) molekular in der Waschflüssigkeit (Absorbens – unbeladen, Absorbat – beladen) gebunden. Die physikalische Bindung wird als Physisorption, die leichte chemische Bindung als Chemisorption bezeichnet. Das Austreiben der nun gebundenen Gaskomponenten kann durch Druckverringerung und/oder Temperaturerhöhung erfolgen. Siehe auch
Kategorien: Trennverfahren | Verfahrenstechnik |
|
| Dieser Artikel basiert auf dem Artikel Absorption_(Physik) aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. |





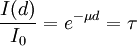
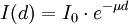
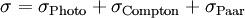 .
.
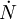 hängt hier hauptsächlich von der Menge eingelagerten Gases
hängt hier hauptsächlich von der Menge eingelagerten Gases