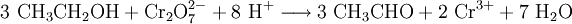Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Alkanole
Als Alkanole bezeichnet man in der organischen Chemie eine Stoffgruppe, die sich von den Alkanen (gesättigten Kohlenwasserstoffen) ableitet. Als funktionelle Gruppe besitzen alle Alkanole eine oder mehrere Hydroxylgruppe(n). Analoge Verbindungen, die sich von ungesättigten Kohlenwasserstoffen ableiten, heißen Alkenole (mit einer oder mehreren Doppelbindungen) sowie Alkinole (mit einer oder mehreren Dreifachbindungen). Das Wort Alkanole stammt aus der IUPAC-Nomenklatur. Die Begriffe Alkohol und Alkanol sind nicht bedeutungsgleich. Der Begriff Alkohol bezieht sich auf die Funktionalität der Hydroxylgruppe, während der Begriff Alkanol darüberhinaus auch den gesättigten Charakter des Alkylrests mit definiert. Weiteres empfehlenswertes Fachwissen
Wertigkeit der AlkanoleSind mehr als eine Hydroxylgruppe in einem Alkoholmolekül vorhanden, wird deren Anzahl durch Einfügen einer der Anzahl der Hydroxylgruppen entsprechenden griechischen Silbe (-di-, -tri-, usw.) vor der Endung -ol angegeben und man spricht von mehrwertigen Alkanolen. Ein Alkandiol ist das Glykol (1,2-Ethandiol), ein Alkantriol das Glycerin (1,2,3-Propantriol). Die Ziffer vor dem Namen des Alkylrestes gibt die Position der funktionellen Gruppe(n) an. Dies gilt auch für einwertige Alkanole, z. B. 2-Propanol (Trivialname Isopropanol). EigenschaftenWichtigstes gemeinsames Merkmal der Alkanole ist die Hydrophilie. Diese Eigenschaft nimmt mit zunehmender Länge des Alkylrestes ab und mit der Anzahl der Hydroxylgruppen zu. Besonders die kurzkettigen Alkanole werden aufgrund ihres amphiphilen Charakters oft als Lösungsmittel verwendet. Homologe ReiheDie Homologe Reihe der n-Alkanole lautet (bis C10): Die allgemeine Summenformel einwertiger Alkanole lautet CnH2n+1OH NachweisDie meisten Nachweisreaktionen beruhen auf der Oxidation der Alkanole zu Aldehyden, Ketone und Carbonsäuren. AlcotestAlkanole reagieren mit (gelb-orangenen) Dichromat-Ionen in stark schwefelsaurer Lösung zu grünem Chrom(III) und Oxidationsprodukten (Alcotest): CertestEine konzentrierte (gelbe) Lösung von Cer(IV)-ammoniumnitrat wird mit einer verdünnten Lösung der unbekannten Substanz versetzt. Anwesenheit von Alkanolen bewirkt einen Farbumschlag nach rot (manchmal auch grün). Grund ist eine Komplexbildung (Ligandensubstitution), bei der ein Alkohol/Phenol mit dem Sauerstoffatom am Cer(IV) zu einem rot/grün/braunen Komplex koordiniert. Lucas-ReagenzDas Lucas-Reagenz erlaubt die Unterscheidung von primären, sekundären oder tertiären Alkanolen. Dabei wird über eine nucleophile Substitution die Hydroxylgruppe mit einem Chloratom ersetzt. Folge ist die Entstehung einer wasserunlöslichen Substanz, die sich abscheidet. Die Geschwindigkeit dieser Phasenbildung entscheidet über die Art des Alkanols:
Kategorien: Stoffgruppe | Alkohol |
|
| Dieser Artikel basiert auf dem Artikel Alkanole aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. |