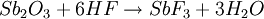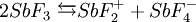Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Antimon(III)-fluorid
Weiteres empfehlenswertes Fachwissen
Gewinnung und DarstellungAntimontrifluorid lässt sich durch Reaktion von wasserfreiem Fluorwasserstoff mit Antimontrioxid herstellen. Hierbei entsteht Antimon(III)-fluorid und Wasser.
EigenschaftenPhysikalische EigenschaftenAntimon(III)-fluorid autodissoziert zu Antimondifluorid- und Antimontetrafluridionen.
Dadurch leitet geschmolzenes Antimontrifluorid auch elektrischen Strom. Die Antimodifluoridionen werden von Antimon(III)-fluorid-Molekülen stabilisiert. Chemische EigenschaftenAntimon(III)-fluorid ist eine starke Lewis-Säure aber eine verhältnismäßig schwache Lewis-Base. Mit Donorfluoriden bildet es Fluorokomplexe. VerwendungAntimon(III)-fluorid wird als mäßig aktives Fluorierungsmittel, bevorzugt für niedrig schmelzende Fluoride, verwendet. Diese lassen sich anschließend vom überschüssigen Antimon(III)-fluorid abdestillieren. Außerdem dient es als Beizmittel zum Färben und wird bei der Herstellung von Keramik verwendet. SicherheitshinweiseAntimon(III)-fluorid ist für den Menschen giftig. Einatmen von Antimon(III)-fluorid kann zu chemischer Lungenentzündung und Lungenödem führen. Berührungen können zu stärken Schädigungen der Haut, der Gewebe der Schleimhäute sowie der Atemwege und der Augen führen. Der LD50-Wert (Maus, oral) beträgt 804 mg/kg. Literatur
Einzelnachweise
Kategorien: Gesundheitsschädlicher Stoff | Umweltgefährlicher Stoff | Antimonverbindung | Fluorid |
||||||||||||||||||||||||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Antimon(III)-fluorid aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. | ||||||||||||||||||||||||||||||||||||||||||||||