Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
BandstrukturDie Bandstruktur beschreibt die Zustände von Elektronen und Löchern eines kristallinen Festkörpers im Impulsraum und damit die Beschaffenheit dessen elektronischer Struktur. Sie ist die Dispersionsrelation von Elektronen unter dem Einfluss des Festkörper-Gitterpotentials. Das Energiebändermodell eines Festkörpers ist im Wesentlichen die im Impulsraum dargestellte Bandstruktur. Weiteres empfehlenswertes Fachwissen
BedeutungDie Bandstruktur zählt zu den zentralen Konzepten der Festkörperphysik. Viele grundlegende Eigenschaften eines Festkörpers können mit Hilfe der Bandstruktur verstanden werden, wie beispielsweise:
Allgemeines
Freie Elektronen der Masse m, ("frei" bedeutet, dass die Elektronen nicht mit anderen Elektronen wechselwirken und sich in keinem Potential befinden [diese Situation wird also durch folgende Hamiltonfunktion beschrieben: Bedingt durch den Einfluss des periodischen Gitterpotentials können Elektronen in einem Festkörper nicht mehr als freie Teilchen angesehen werden. Im einfachsten Fall wird das durch die abweichende effektive Masse m* berücksichtigt, was zu Parabelkurven verschiedener Steilheit führt. Die vollständige Dispersionsrelation der Kristallelektronen wird durch die Bandstruktur beschrieben: Diese stellt die Energie über dem Wellenvektor Ein Energieband, wie beispielsweise das Leitungs- oder Valenzband, ergibt sich durch den Energiebereich, welche die zugehörige Direkte und indirekte ÜbergängeBei Übergängen, die ohne Änderung des Impulsvektors k erfolgen, also im Diagramm senkrecht, spricht man von direkten Übergängen. Ansonsten handelt es sich um indirekte Übergänge. Bei Halbleitern spricht man je nach dieser Natur ihrer Fundamentalabsorption von direkten oder indirekten Halbleitern. DarstellungsartenTrägt man die Wellenfunktion der Elektronen in einem Energie-Wellenzahl-Diagramm auf, so erhält man in Richtung des Impulsraums abwechselnd erlaubte Energiebereiche (Energiebänder) und verbotene Energiebereiche (Energielücken). Ebenso können Überlappungen von Energiebändern auftreten (z. B. bei mehrwertigen Metallen). Es gibt drei Varianten von Bandstrukturdiagrammen (auch als Zonenschemen oder Energie-Wellenzahl-Diagramme bezeichnet):
Bandstrukturen realer FestkörperBandstrukturen realer Kristalle können sehr komplex sein (Beispiel: GaAs und AlAs [1]). Üblicherweise stellt man die Dispersionsrelation in einem eindimensionalen Schema dar, wobei die Verbindungslinien zwischen verschiedenen charakteristischen Punkten der Brillouin-Zone einfach aneinandergehängt werden. In jedem realen Kristall gibt es im Energiebereich der Bandlücke zusätzliche lokalisierte Zustände, die von Verunreinigungen, Gitterfehlern oder Oberflächeneffekten herrühren. Diese Zustände können systematisch erzeugt und für Anwendungen genutzt werden, z. B. beim Dotieren von Halbleitern oder in Farbzentren. Siehe auch |
|
| Dieser Artikel basiert auf dem Artikel Bandstruktur aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. |





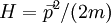 ]), besitzen eine parabolische Dispersionsrelation, d. h. der Zusammenhang zwischen
]), besitzen eine parabolische Dispersionsrelation, d. h. der Zusammenhang zwischen 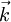 und Energie
und Energie 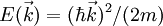 .
.
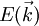 -Kurve überdeckt (vgl. Abbildung): Für diese Energien gibt es erlaubte Zustände im Impulsraum. Der Bereich der
-Kurve überdeckt (vgl. Abbildung): Für diese Energien gibt es erlaubte Zustände im Impulsraum. Der Bereich der 

