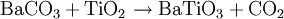Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Bariumtitanat
Bariumtitanat ist ein Mischoxid von Barium und Titan und kristallisiert in der Perowskit-Struktur. Weiteres empfehlenswertes Fachwissen
Gewinnung/DarstellungBaTiO3 kann nach der klassischen Mischoxid-Methode aus BaCO3 und TiO2 in einer Festkörperreaktion, dem sogenannten Kalzinieren, bei einer Temperatur von 1200 °C hergestellt werden. Moderatere Bedingungen bietet die Kristallisation aus schmelzflüssiger Lösung. Stöchiometrische Mengen Bariumcarbonat und Titandioxid (Anatas) werden mit einem großen Überschuss Natriumchlorid vermengt. Im Ofen kristallisiert bei 1.000 °C das Bariumtitanat aus. Nach Auswaschen der Salzreste erhält man es in sehr reiner Form, in feinen Kristallen. EigenschaftenPhysikalische EigenschaftenBariumtitanat gehört zur Gruppe der Elektrokeramiken. Bariumtitanat ist ein Ferroelektrikum und besitzt eine ausgeprägte Hystereseschleife. Wie alle Ferroelektrika besitzt es eine hohe Dielektrizitätskonstante von über 2.000. Bariumtitanat kristallisiert in zwei polymorphen Gitter-Typen, dem hexagonalen Gitter-Typ und der Perowskit-Struktur. Bei Temperaturen < 120 °C liegt es als tetragonal verzerrte Modifikation der Perowskit-Struktur vor bei der das Titanion gegenüber den Sauerstoffionen in z-Richtung verschoben ist. Daraus resultiert ein Dipolmoment der Einheitszelle und die Polarisation. Bei 120 °C erfolgt die Phasenumwandlung zur kubischen Perowskit-Struktur, bei der sich das Titanion genau im Zentrum des Oktaeders aus Sauerstoffionen befindet. Damit hat die Einheitszelle des Kristalls kein Dipolmoment mehr und der Kristall ist nicht mehr ferroelektrisch. Bei hohen Temperaturen erfolgt die Phasenumwandlung in die hexagonale Phase. Diese Phasenumwandlung erfordert eine umfangreichere Umordnung der Ionen als der Übergang bei 120 °C. Bei größeren Kristallen kommt es deshalb häufig vor, dass sie bei dieser Umwandlung zerbrechen. VerwendungAufgrund der ferroelektrischen, dielektrischen und pyroelektrischen Eigenschaften findet Bariumtitanat sowie verwandte Perowskite wie Pb(Zr,Ti)O3 vielseitige Anwendung in der Elektronik und Sensorik. Als Beispiel seien hierzu Kaltleiter, sowie die Verwendung als Dielektrikum in Kondensatoren, insbesondere in Keramikkondensatoren erwähnt. Literatur
Quellen
Kategorien: Gesundheitsschädlicher Stoff | Oxidkeramik | Bariumverbindung | Titanverbindung |
|||||||||||||||||||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Bariumtitanat aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. | |||||||||||||||||||||||||||||||||||||||||