Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
CarbideCarbide sind binäre Verbindungen eines Elements E mit Kohlenstoff C zu Verbindungen des Typs ExCy. Weiteres empfehlenswertes Fachwissen
AllgemeinesHergestellt werden die Carbide in der Regel aus elementarem Kohlenstoff, welcher bei hohen Temperaturen mit dem entsprechenden Element, Elementoxid oder Elementcarbonat in einer Festkörperreaktion umgesetzt wird. Die Herstellung von Calciumcarbid aus Koks C und Calciumcarbonat CaCO3 beispielsweise erfolgt bei 2000 °C im Drehrohrofen. 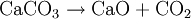
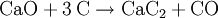 Abhängig von der Elektronegativitätsdifferenz zwischen dem betreffenden Element und Kohlenstoff werden dabei unterschiedliche Typen von Carbiden ausgebildet. Ionische CarbideIonische Carbide haben starken Salzcharakter und werden typischerweise von den stark elektropositiven Elementen der Alkali-, Erdalkali- und Erdelemente ausgebildet. Es sind damit chemische Verbindungen, die Kohlenstoff als elektronegativeren Bestandteil enthalten. Typische Beispiele sind Lithiumcarbid Li4C, Berylliumcarbid Be2C, Magnesiumcarbid Mg2C3, Calciumcarbid CaC2 oder Aluminiumcarbid Al4C3. Sie enthalten in ihrem Ionengitter das jeweilige Metallkation sowie das Carbidion, welches sich formal von verschiedenen Kohlenwasserstoffen ableitet. Dies führt zu einer weiteren Differenzierung der Carbide in die Methanide (Li4C, Be2C und Al4C3 enthalten C4- abgeleitet von Methan CH4), die Acetylide (z.B. CaC2 enthält (C22- abgeleitet von Ethin (Acetylen) C2H2) und Allenide (z.B. Mg2C3 enthält C34-, abgeleitet von Allen C3H4). Ionische Carbide reagieren mit Wasser unter Bildung des entsprechenden Metallhydroxids und dem entsprechenden Kohlenwasserstoff, welcher durch vielfache Protonierung durch das Wasser frei gesetzt wird. Der bekannteste Vertreter ist das in der Karbidlampe verwendete Calciumcarbid (CaC2), oft einfach Karbid genannt, welches bei Anwesenheit von Wasser Ethin freisetzt: 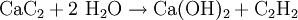 Die graue Farbe des eigentlich weißen Calciumkarbids resultiert aus Verunreinigungen an elementarem Kohlenstoff aus dem Herstellprozess (siehe oben). Der typische Geruch des Calciumcarbids ist dem Monophosphan PH3 zuzuschreiben, welches in analoger Weise zum Acetylen durch Hydrolyse aus Calciumphosphid gebildet wird. Calciumphospid entsteht im Herstellprozess, wenn das eingesetzte Calciumkarbonat Spuren von Calciumphosphat als Verunreinigung beinhaltet. Die Hydrolyse von Calciumcarbid war bis in die dreißiger Jahre des zwanzigsten Jahrhunderts die einzige Möglichkeit im technischen Maßstab Ethin herzustellen und ist somit ein wichtiger Ausgangsstoff für die Entwicklung der Acetylen-Chemie (vgl. Reppe-Chemie) gewesen. Mit dem Aufkommen der petrochemischen Industrie hat diese Ethin-Quelle jedoch heute enorm an Bedeutung verloren. Kovalente CarbideDie kovalenten Carbide werden zwischen Kohlenstoff und Elementen mit annähernd gleicher Elektronegativität gebildet. Die beiden wichtigsten Beispiele sind SiC (Siliciumcarbid, „Carborundum®“) und B4C (Borcarbid). Sie bestehen aus kovalenten Bindungen zwischen Kohlenstoff und dem jeweiligen Element. Die Ausbildung der sehr starken kovalenten Bindungen, verbunden mit einer Kristallstruktur, die harten Stoffen sehr ähnelt (SiC besitzt Diamantstruktur) führt zu einer hohen mechanischen Stabilität. Demgemäß finden diese Carbide in der Regel als Hartstoffe (Beschichtungen, Schleifwerkzeuge) und zur Verstärkung von Kunststoffen Verwendung. Siliciumcarbid ist auch als Trägermaterial für Katalysatoren in der chemischen Industrie von Interesse, da es eine hohe Wärmeleitfähigkeit und praktisch keinen Abrieb besitzt. Metallartige CarbideDiese Carbide werden von den Elementen der 4.–7. Nebengruppe gebildet, typische Beispiele sind Titan und Wolfram. Sie besitzen in der Regel keine exakt definierte Stöchiometrie. Grund hierfür ist, dass einzelne Kohlenstoffatome in die Tetraederlücken der Metallgitter eingelagert werden (sogenannte Einlagerungsverbindungen oder interstitielle Verbindungen). Die entstehenden Substanzen zeichnen sich wiederum durch eine hohe mechanische und thermische Stabilität und hohe Schmelzpunkte (3000−4000 °C) aus und dienen als Hartstoffe und Keramiken im chemischen Apparate- und Anlagenbau sowie als Schneide- und Schleifwerkzeuge. Die Kugel eines Kugelschreibers besteht beispielsweise aus Wolframcarbid. CarbidschießenDie Tradition des Carbidschießens wird vornehmlich in Holland und in einigen Teilen Nordwestdeutschlands und nord Bayerns von jungen Männern zu Hochzeiten, Silvester und Neujahr gepflegt. In der Oberlausitz ist es als Osterschießen bekannt. Durch das hohe Gefahrenpotenzial ist das Carbidschießen in Deutschland verboten und in Holland nur an Silvester und Neujahr gestattet, aber es wird in Deutschland auch noch von Jugendlichen an Silvester oder ähnlichen Veranstaltungen praktiziert. In den Niederlanden werden dabei regelrechte Carbidschießfeiern abgehalten. Legt man einige Calciumcarbidstücke in eine Milchkanne und beträufelt man es mit ein bisschen Wasser, so entsteht in dem mit einem Deckel oder Fußball abgedichtetem Volumen ein explosives Gasgemisch. Das Gasgemisch wird dann durch ein zuvor gebohrtes Loch im Boden entzündet. Durch die Explosion kann der Deckel oder Fußball bis zu 70m weit geschleudert werden. CarbidfischenDas gleiche Prinzip machten sich in der Hungerzeit nach dem Weltkrieg einige Personen zunutze, um trotz Verbots der Besatzungsmächte durch Explosion einer Carbiddose in Fischgewässern rasch viele Fische zu töten und abzuräumen "bevor der Jeep kommt". Karbid war wegen der Verwendung zur Acetylenherstellung fürs Schweißen und wegen der Verwendung in Karbid-Fahrradlampen damals leicht verfügbar. Siehe auch
Kategorien: Stoffgruppe | Carbid |
|
| Dieser Artikel basiert auf dem Artikel Carbide aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. |







