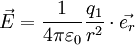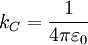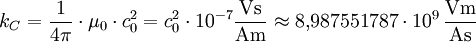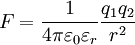Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Coulombsches GesetzDas Coulomb-Gesetz (nach Charles Augustin de Coulomb, 1785) bildet die Basis der Elektrostatik und beschreibt die Kraft zwischen zwei kugelsymmetrisch verteilten elektrischen Ladungen. Es besagt, dass der Betrag dieser Kraft proportional zum Produkt der beiden Ladungsmengen und umgekehrt proportional zum Quadrat des Abstandes der Kugelmittelpunkte ist. Die Kraftrichtung wirkt je nach Vorzeichen der Ladungen anziehend oder abstoßend in Richtung der Verbindungsgeraden der Mittelpunkte. Bei mehr als zwei Ladungen werden die einzelnen Kraftvektoren addiert (Superposition). Weiteres empfehlenswertes FachwissenCoulomb-Kraft im VakuumDas Coulomb-Gesetz wurde von Coulomb um 1785 entdeckt und in umfangreichen Experimenten verifiziert. Im Internationalen Einheitensystem und in skalarer Form ist die Kraft demnach
wobei q1 und q2 zwei jeweils kugelsymmetrisch verteilte Ladungsmengen, r der Abstand zwischen deren Mittelpunkten und
Hierbei ist Weiter ist der Vektor der Feldstärke des von der Ladung q1 erzeugten elektrischen Feldes im Abstand r vom Mittelpunkt. Die Konstante wird auch als Coulomb-Konstante bezeichnet. Es gilt: Im Gaußschen und elektrostatischen CGS-Einheitensystem wird das Coulomb-Gesetz zur Definition der elektrischen Ladung benutzt. Eine Ladungseinheit wirkt auf eine zweite im Abstand 1 cm mit der Kraft 1 dyn. Die elektrische Basiseinheit der Einheitensysteme SI, CGS-ESU und CGS-EMU unterscheidet sich prinzipiell nur durch die Festlegung von µ0:
Coulomb-Kraft in einem MediumDas Coulomb-Gesetz lässt sich auf einfache Weise auf den Fall von Ladungen in homogenen, isotropen, linearen Medien erweitern. Das die Ladungen umgebende Material muss sich dazu in guter Näherung diese Eigenschaften besitzen:
Insbesondere verlangt die Homogenität, dass der atomare Charakter der Materie im Vergleich zum Abstand der Ladungen vernachlässigbar ist. Für solche Medien schreibt sich das Coulomb-Gesetz in gleicher Form wie im Vakuum, mit dem einzigen Unterschied, dass ε0 durch ε = ε0·εr ersetzt wird. Die relative Permittivität εr ist bei isotropen Medien eine Materialkonstante, die der Polarisierbarkeit des Mediums Rechnung trägt. Sie kann sowohl durch Messungen als auch aus theoretischen Überlegungen gewonnen werden. In der Umkehrung gilt im Vakuum εr = 1.
Literatur
|
| Dieser Artikel basiert auf dem Artikel Coulombsches_Gesetz aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. |





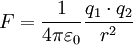 ,
,
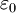 die
die 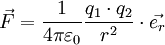 .
.
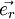 ein Einheitsvektor in Richtung der Verbindungslinie der Ladungsmittelpunkte. Dabei gilt, dass sich Ladungen mit gleichem Vorzeichen (gleichnamige Ladungen) abstoßen und solche mit verschiedenem Vorzeichen (ungleichnamige Ladungen) anziehen.
ein Einheitsvektor in Richtung der Verbindungslinie der Ladungsmittelpunkte. Dabei gilt, dass sich Ladungen mit gleichem Vorzeichen (gleichnamige Ladungen) abstoßen und solche mit verschiedenem Vorzeichen (ungleichnamige Ladungen) anziehen.