Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
DünnschichtchromatografieDie Dünnschichtchromatografie, oft einfach DC abgekürzt, ist ein physikalisch-chemisches Trennverfahren, das zur Untersuchung der Zusammensetzung von Proben genutzt wird, zum Beispiel auch zum raschen Nachweis ihrer Reinheit und Identität. Lösungen von bekannten Vergleichskomponenten werden dabei oft gleichzeitig mit der eigentlichen Probe untersucht und dienen zur sicheren Identifizierung der chemischen Verbindungen in der Probe. Grundlage der Methode sind Wanderungsprozesse in einer Flüssigkeit, die durch eine Pulverschicht strömt. Dabei zeigen unterschiedliche Moleküle meist unterschiedliches Wanderungsverhalten (Bsp. Aminosäuren). Die Methode ist vielfältig einsetzbar und weit verbreitet. Alle Proben, die ausreichend stabil sind und in Lösung gebracht werden können, lassen sich untersuchen. Der Erfolg hängt davon ab, wie groß die Unterschiede beim Wanderungsverhalten der interessierenden Moleküle sind. Es ist auch notwendig, dass Methoden zur Verfügung stehen, die die in der Regel farblosen Moleküle sichtbar machen. Untersucht werden zum Beispiel Probelösungen von Naturstoffen, Medikamenten, Reaktionsmischungen und Reaktionsprodukten im chemischen Labor. Im größeren Maßstab dient die Methode auch zur Gewinnung und Weiterverarbeitung von Probekomponenten: "präparative Dünnschichtchromatografie" (bzw. auch Dickschichtchromatografie). Oberbegriffe sind Flüssigchromatografie und Chromatografie.
Weiteres empfehlenswertes Fachwissen
Geschichte [1]N. A. Izmailov und M. S. Shraiber, zwei russische Forscher, führten 1938 eine chromatographische Trennung mit einer horizontalen Dünnschichtplatte durch, auf die sie das Lösemittel auftropften. Doch ihre Methode wurde kaum beachtet. Erst als J. G. Kirchner und seine Mitarbeiter (darunter auch B. Harnischmacher) sich ab 1951 mit ihr befassten, wurde das Interesse anderer an der Methode geweckt. Zum Durchbruch verhalf ihr E. Stahl, als er die Herstellung von leistungsfähigen Platten beschrieb. Von ihm stammt auch der Name Dünnschichtchromatografie. TrennvorgangAuftragenMan gibt eine kleine Menge der zu untersuchenden, verdünnten Probelösung als punktförmigen Tropfen oder kurzen Strich aus einer Kapillare auf eine dünne Schicht aus sehr feinkörnigem Material (z. B. Kieselgel, Kieselgur, Aluminiumoxid, Cellulose), die Trennschicht oder auch stationäre Phase genannt wird. Diese Trennschicht ist sehr gleichmäßig auf eine Trägerfolie oder Trägerplatte aus Kunststoff, Aluminiumblech oder Glas aufgetragen und kommerziell in unterschiedlichen Schichtdicken erhältlich. Auf die DC-Folie wird auf der Startlinie (meist einmal oder zweimal am unteren Rand der Folie; im Fall der 2-dimensionalen DC einmal in der unteren linken Ecke) das zu untersuchende Gemisch aufgetragen und in die DC-Kammer mit dem Laufmittel gegeben. (Nach einem ersten Chromatografie-Prozess kann nach Abdampfen des Laufmittels, Drehen der Folie um 90 Grad, Wechsel des Laufmittels und neuerlicher Chromatografie eine so genannte 2-dimensionale Auftrennung erreicht werden. Vorteil: bessere Auftrennung bei Multikomponentengemischen, Nachteil: Identifizierung schwieriger.) Daneben werden auf der Startlinie in vielen Fällen auch Lösungen von reinen Vergleichssubstanzen oder Vergleichsmischungen aufgetragen (Lösungen verdünnt, etwa einprozentig). Es ist entscheidend, die Auftragzonen möglichst eng zu halten (ein bis drei Millimeter maximal). Kommerziell erhältlich sind auch DC-Folien mit so genannten Konzentrationszonen. Damit sind so besonders enge Auftragzonen erzielbar. Die Probeflecken werden dadurch nach Beginn der Chromatografie in der Richtung der Laufstrecke zusammengestaucht (Zone mit geringer Adsorption wird vorgeschaltet). AuftrennungNun stellt man dieses Trennsystem senkrecht in ein Gefäß mit einem geeigneten Fließmittel, der mobilen Phase, in die die DC-Folie zu einem geringen Teil eintaucht, und verschließt es. Als Laufmittel wird meist eine Mischung eines unpolaren und eines mäßig polaren organischen Lösungsmittels genutzt (z.B. Petrolether und Essigsäureethylester). Über das Mischungsverhältnis kann man somit die Polarität des Fließmittels gut steuern. Das Fließmittel saugt sich nun über Kapillarkräfte in die stationäre Phase nach oben. Sobald die Flüssigkeit den Gemischfleck erreicht hat, wird er gelöst; seine Moleküle sind nun den Anziehungskräften der stationären Phase einerseits und den Anziehungskräften der mobilen Phase andererseits ausgesetzt. Je nach Kräfteverhältnis bleibt ein Teilchen eher am Startpunkt oder es wandert eher mit der mobilen Phase nach oben. Im Allgemeinen gilt: Je polarer das Fließmittel ist, desto weiter wandern polare Substanzen, und umgekehrt. Durch unterschiedliche Wechselwirkungen der Komponenten des aufgetragenen Gemischs mit der stationären und der mobilen Phase trennt sich die Mischung auf. Um eine Beeinflussung der Ergebnisse durch das Verdampfen des Fließmittels zu verhindern, führt man die Trennung in einer mit dem Fließmittel gesättigten Atmosphäre in einem geschlossenen Gefäß durch. Die Kräfte und somit das Wanderverhalten eines Teilchens hängen sowohl von der Art des Schichtmaterials und des Fließmittels, als auch von der Art des Teilchens ab. In den meisten Fällen lassen sich Schichtmaterialien und Fließmittelgemische so kombinieren, dass die verschiedenen Teilchensorten eines Gemisches verschieden weit wandern, sodass sie sich von einander trennen lassen. PhasenverhältnisseBei einer genaueren Analyse dieses Begriffes sollte man von einem Wettkampf zwischen den diversen Probemolekülen mit den Molekülen des Fließmittels (Laufmittels) um die Haftstellen des Adsorbens sprechen. In der Regel handelt es sich dabei um polare Haftstellen (z.B. bei Kieselgel). Sehr interessant ist auch die Verwendung von DC-Material, bei dem Adsorbentien eingesetzt werden, die unpolare Haftstellen aufweisen ("reversed phase" im Gegensatz zur "normal phase"). Die Reihenfolge, in der die verschiedenen Probemoleküle aufgetrennt werden ist dabei in der Regel umgekehrt (die polaren Moleküle kommen rascher). Vorteilhaft ist dabei unter anderem, dass auch sehr polare Proben untersucht werden können oder Proben unmittelbar aus wässriger Lösung heraus (die Polarität des Fließmittels ist im allgemeinen ebensfalls höher). Es gibt auch DC-Material mit speziellen chemischen Gruppen im Adsorbens (so genannte chemisch gebundene Phasen) für Spezialanwendungen. Grundprinzip der AuftrennungDas Grundprinzip der Chromatografie kann folgend verstanden und zusammengefasst werden: Moleküle verteilen sich auf zwei Phasen in einem bestimmten Verhältnis (Gleichgewichtszustand). Entscheidend ist, dass sie individuell sehr rasch von der einen Phase in die andere wandern (auf Grund der Wärmebewegung, der Diffusion und der raschen Austauschprozesse) und wieder zurück (dynamischer Gleichgewichtszustand). Der Zeitanteil, den das individuelle Molekül in der mobilen (bzw. der stationären) Phase zubringt, entspricht auch genau dem Anteil der Moleküle dieser Molekülsorte in den beiden Phasen. Diese Verhältnisse gelten auch, wenn die "mobile" Phase nicht bewegt wird. Der "Trick" der Chromatografie besteht einfach darin, die Unterschiede, die es bei diesen Austauschvorgängen zwischen den verschiedenen Molekülsorten (Verbindungen, auch Ionen) gibt, in Geschwindigkeitsunterschiede zu verwandeln. Die Geschwindigkeit ergibt sich einfach aus dem Produkt der Geschwindigkeit der mobilen Phase und dem Zeitanteil, den die Probemoleküle in der mobilen Phase verbringen. Es wird angenommen, dass die Moleküle in der mobilen Phase (statistisch gesehen) dieselbe Geschwindigkeit haben wie die Laufmittelmoleküle. Sind sie an die stationäre Phase gebunden, ist die Geschwindigkeit gleich Null ("stop and go"-Modell). So werden also Verteilungsunterschiede (Verteilung im allgemeinen Sinn) in Geschwindigkeitsunterschiede verwandelt. Oft sind die Verteilungsunterschiede nur gering. Auftrennungen wären so mit anderen Methoden kaum zu erzielen. In dem Augenblick, in dem es sich aber um Geschwindigkeitsunterschiede handelt, ist es nur eine Frage der Zeit, die für das Experiment zur Verfügung steht bzw. der Länge der Wegstrecke, bis es zu einer ausreichenden Auftrennung gekommen ist. ZonenverbreiterungBestimmte statistische Umstände wirken einer guten Auftrennung entgegen. Entscheidend ist der rasche Wechsel der Probemoleküle zwischen Phase 1 und Phase 2. Daher ist es auch günstig, möglichst geringe Abstände zu haben (und feine, einheitliche Korngrößen des Schichtmaterials). Das ist auch günstig, um die Unterschiede der gesamten Wegstrecke, die für eine bestimmte Molekülart auftreten, gering zu halten ("Zickzack-Weg"). Zu geringe und zu hohe Geschwindigkeiten der mobilen Phase wirken sich negativ aus. Eine zu geringe Geschwindigkeit begünstigt eine Vergrößerung der Zonen, in denen sich die Probemoleküle aufhalten. Je mehr Zeit zur Verfügung steht, desto größer ist die Rolle, die Diffusionsprozesse innerhalb der mobilen Phase spielen. - Dabei kann man zum Beispiel an die Vergrößerung des Volumens einer Tintenlösung denken, die von reinem Wasser umgeben wird. Je mehr Zeit verstreicht, desto größer ist die Ausdehnung (auch wenn es keine Erschütterungen gibt. - Ist die Geschwindigkeit zu hoch, kommt es seltener zu einem Wechsel der Probemoleküle zwischen den Phasen 1 und 2. Das führt zu einer größeren statistischen Streuung und ist ebenfalls unerwünscht. Bei allen chromatografischen Methoden gibt es entsprechend eine optimale Geschwindigkeit der mobilen Phase (siehe auch Van-Deemter-Gleichung). Je feiner die Korngrößen sind (bzw. die Dimensionen), desto größer kann sie werden. Das ist auch ein ökonomischer Vorteil. Bei der DC ist die erwünschte räumliche Auftrennung zwischen den verschiedenen Probekomponenten der gesamten Laufstrecke proportional (Abstand Startlinie - "Laufmittelfront"). Die Vergrößerung der einzelnen Zonen auf Grund statistischer Effekte ist geringer (nicht der Laufstrecke proportional sondern der Wurzel der Laufstrecke). Daher ist es bei schwierigen Trennungen sinnvoll, größere DC-Folien und Laufstrecken zu verwenden. Nachweis
Die getrennten Substanzen müssen in der Regel durch Besprühen mit Reagenzien-Lösungen sichtbar gemacht (detektiert) werden. Alternativ ist bei der Anwendung auch Tauchung in Lösungen möglich. Oft handelt es sich dabei um Farbreaktionen, die sich empfindlich und spezifisch zum Nachweis bestimmter funktioneller Gruppen eignen. Über die Auswahl der Farbreaktion lässt sich der Informationsgehalt bei der DC wesentlich erhöhen. Alternativ werden Reaktionen eingesetzt, die allgemein wirksam sind (zum Beispiel Oxidation mit Hilfe von Salpetersäurelösungen). Bei einer Reihe von Farbreaktionen ist es erforderlich, die Folie nach dem Besprühen bzw. der Tauchung zu erhitzen. Viele Schichtmaterialien enthalten Zusätze, die im UV-Licht fluoreszieren und an denjenigen Stellen dunkle Fluoreszenzquenchung ("Fluoreszenzlöschung") zeigen, an denen sich die getrennten Stoffe befinden. Diese Fluoreszenzfarbstoffe dürfen während der chromatografischen Trennung nicht wandern. Gebräuchlich sind vor allem Mangan aktiviertes Zinksilikat (mit UV-Licht der Wellenlänge 254 nm bestrahlt) und Calciumwolframat (mit UV-Licht der Wellenlänge 366 nm bestrahlt). Tatsächlich handelt es sich bei der Methode nicht um eine Fluoreszenzlöschung im engeren Sinne. Probemoleküle werden sichtbar, wenn sie im Bereich von 254 nm oder 366 nm UV-Licht absorbieren (je nach verwendeter UV-Lampe). Es gelangt dann weniger UV-Licht zu den Fluoreszenzfarbstoffmolekülen (dunkle Flecken auf grün bzw. blau leuchtendem Hintergrund zu sehen). Dazu müssen genügend viele funktionelle Gruppen bzw. genügend große Systeme mit konjugierten Doppelbindungen vorhanden sein. Gesättigte Kohlenwasserstoffe und viele Aminosäuren sind daher mit dieser Methode nicht nachzuweisen, aromatische Verbindungen z.B. sehr leicht (bei 254 nm). Auch die Eigenfluoreszenz bestimmter Stoffe oder andere Eigenschaften wie Radioaktivität können zur Detektion herangezogen werden (Bestrahlung mit UV-Licht bei 254 oder 366 nm). Eine weitere, sehr einfache Methode besteht in der Bedampfung mit molekularem Iod. Dazu genügt es, in ein Glasgefäß ein paar Iod-Kristalle zu legen. Sie sublimieren, das heißt sie verdampfen direkt bei Raumtemperatur, bilden einen violetten Dampf von Diiodmolekülen. Durch Einlegen einer DC-Folie in einen solchen Trog werden über Diffusion und Reaktion mit den Molekülen der Substanzflecken binnen kurzer Zeit lockere Komplexverbindungen gebildet (lila oder braun). Vorteil bzw. Nachteil der Methode: die Iod-Verbindungen zerfallen relativ rasch. Sinnvoll und gebräuchlich ist eine Kombination von Methoden: zuerst Betrachtung unter der UV-Lampe, anschließend chemische Reaktionsmethoden. In der Biochemie ist eine saure Ninhydrin-Lösung ein häufiges Sprühreagenz, um Aminosäuren zu detektieren. Hierbei wird das Ninhydrin über die Schiffsche Base und durch eine Decarboxylierung sowie Hydrolyse zu Ruhemans Violett. Durch Auftragen von Referenzproben, welche unter gleichen Bedingungen gleich weit wandern wie entsprechende Probekomponenten, kann man das qualitative Auftreten von Stoffen nachweisen. Hierzu wird die Lage der verschiedenen Punkte mit der Lage der Referenzproben verglichen. Neben dieser qualitativ schnellen Nachweismethode von Aminosäuren gibt es auch noch andere chromatographische Nachweismethoden von Aminosäuren wie z.B. Ionenaustauschchromatografie und Reversed Phase HPLC. Um verschiedene DCs vergleichen zu können werden die so genannten Rf-Werte (Retentionsfaktor) berechnet. Es handelt sich dabei um das Verhältnis Wanderungsstrecke des Substanzfleckes (S) zur Wanderungsstrecke des Lösemittels (L): Präparative DCDie DC (engl.: TLC Thin Layer Chromatography, frz.: CCM) kann auch präparativ genutzt werden. Hierzu werden auf dickere stationäre Phasen relativ große Mengen der zu trennenden Substanzmischung in einem Strich aufgetragen. Nach dem Trennlauf bilden sich idealerweise zwei oder drei völlig voneinander getrennte Striche in verschiedenen Höhen, die dann z.B. durch mechanisches Abkratzen in verschiedene Gefäße verteilt und separat eluiert werden. Für bestimmte, besonders empfindliche Analyseverfahren (Massenspektrometrie, Infrarotspektroskopie) lassen sich auch die üblichen dünnen (analytischen) DC-Folien präparativ nutzen. Empfehlenswert ist auch die so genannte zirkulare Dünnschichtchromatografie. Dabei werden kreisförmige Glasscheiben beschichtet (eine Kreiszone). Das Schichtmaterial enthält einen Fluoreszenzfarbstoff (der bei UV-Licht der Wellenlänge 254 nm oder 366 nm fluoresziert). Die Probelösung wird mit Hilfe einer Pumpe zum inneren Rand der Schicht geleitet, vorher und nachher das entsprechende Fließmittel. Die Scheibe sitzt dabei auf einem Rotor auf und wird mit Hilfe eines Elektromotors in rasche und gleichmäßig kontrollierte Rotation versetzt. Zur Beobachtung wird der Trennvorgang unter Bestrahlung mit einer UV-Lampe kontrolliert. Am Anfang des Trennprozesses befindet sich die Probe in einer wenige Millimeter starken Kreiszone am inneren Rand der Scheibe. Im Lauf der Zeit zerlegt sich die Probe in eine Reihe von Ringen, die nach außen wandern. Wenn eine Probenkomponente am äußeren Rand der Schicht angelangt ist, wird sie zusammen mit dem Laufmittel in einen Kunststoffreifen zentrifugiert (auf Grund der raschen Rotation), der die Führung der Scheibe umgibt. Die Achse der Scheibe ist während der Chromatografie schräg gestellt, das "Eluat" rinnt am unteren Ende des Kunststoffreifens zusammen und über eine Öffnung und einen Schlauch in entsprechende Sammelbehälter. Die Methode hat eine Reihe von Vorteilen (gegenüber normaler DC und gegenüber der üblichen präparativen Säulenchromatografie): 1. Es können größere Mengen aufgetrennt werden als mit normaler Dickschichtchromatografie (bei geringerem Zeitaufwand). 2. Die Oberfläche der Schicht kann gut zugeschliffen werden (einheitliche Schichtdicke). 3. Das kostspielige Schichtmaterial wird gut für den Trennprozess ausgenützt ("Geometrie" ist ideal). 4. Es ist einfach möglich, während der Chromatografie die Polarität des Laufmittels (Fließmittels) zu erhöhen. Davon wird gerne Gebrauch gemacht. Damit lassen sich auch Mischungen zerlegen, die Substanzgruppen enthalten, die sich voneinander stark in der Polarität unterscheiden. 5. Am Schluss ist es einfach möglich, die Schicht durch längeres Auswaschen mit einer polaren Laufmittellösung wieder zu reinigen. Der Reinigungsprozess lässt sich gut verfolgen (UV-Lampe). Im Gegensatz zur Regeneration bei Säulenchromatografie-Methoden kann diese "Waschflüssigkeit" leicht entfernt werden: Abdampfen lassen, trocknen und aktivieren in einem elektrischen Ofen (ca. 50 bis 60 Grad Celsius). 6. Der Fortgang der Chromatografie kann ständig verfolgt werden. Die Aufsammlung der Probekomponenten wird dadurch erleichtert (das "Schneiden" der Fraktionen). Der Trennprozess lässt sich adaptieren, entsprechend der laufenden Beobachtung. 7. Die Aufgabe der Probe ist einfacher zu gestalten als bei der normalen präparativen DC. Durch Verwendung eines Lösungsmittels mit niedriger Polarität lässt sich eine besonders enge ("scharfe") Startzone erreichen. Nachteile: 1. Bei luft- und UV-licht-empfindlichen Verbindungen kann es Probleme geben. Unter Umständen kann auch unter Schutzgas gearbeitet werden. 2. Eine Reihe von Vorteilen fällt weg, wenn die Verbindungen nicht mit der Fluoreszenzfarbstoffmethode sichtbar gemacht werden können. 3. Die Anschaffungskosten des Gerätes sind relativ hoch (im Vergleich zu einfachen DC-Trögen). Die Kunststoffteile bestehen aus Teflon. Vorteile und Nachteile der DünnschichtchromatografieIm Gegensatz zu den leistungsfähigeren Chromatografie-Verfahren wie Gaschromatografie und HPLC kommt die DC mit geringem apparativen Aufwand aus und stellt sich als schnelles, vielseitiges und preiswertes Analyseverfahren dar. Die Gaschromatografie lässt sich nur bei Proben anwenden, die unzersetzt verdampfbar sind. Bei der Flüssigchromatografie gibt es wenig Einschränkungen. Fast immer lässt sich ein Weg finden, eine Probe aufzulösen. Im Vergleich zu den säulenchromatografischen Methoden besteht der Vorteil, dass Proben, die Gruppen von Komponenten enthalten, die sich jeweils stark in der Polarität unterscheiden, leichter zu erfassen sind. Laufmittelwechsel ist nicht so leicht möglich wie bei der Säulenchromatografie. Es ist aber möglich, zunächst in einem Laufmittel zu entwickeln und nach Zwischentrocknung in einem anderen (das sich in der Polarität stark unterscheidet). Nachteilig ist bei der analytischen Anwendung der DC, dass es schwerer ist, eine quantitative Analyse durchzuführen. Bei bestimmten Aufgabestellungen genügt es allerdings schon, die Mengenverhältnisse abzuschätzen (Fortschritt einer chemischen Reaktion z.B.). Beispielexperiment: Dünnschichtchromatografie von BlattfarbstoffextraktDurch dünnschichtchromatografische Untersuchungen von Blattfarbstoffextrakt kann man erkennen, aus welchen Farb-Komponenten er besteht: Carotinen, Chlorophyllen und Xanthophyllen. Versuchsmaterial
Herstellung des Chlorophyllextraktes/ Isolierung der Blattpigmente Ca. 5 Gramm Blattmaterial werden unter Verwerfung der starken Blattrippen sowie der Stiele in kleine Stücke zerrissen und in den Mörser gelegt. Zum zerkleinerten Blattmaterial wird das Calciumcarbonat hinzugegeben, dies dient der Neutralisation des sauren Zellsaftes. Daraufhin kommt Seesand in den Mörser, um die Blattstücke aufschließen zu können. Nach der Zugabe von Aceton wird das Material im Mörser einige Minuten zerrieben. Wenn eine kräftig dunkelgrün gefärbte Lösung entstanden ist, wird sie in einen Erlenmeyer-Kolben abfiltriert. VersuchsdurchführungDer gewonnene Blattfarbstoffextrakt wird mit einem Kapillarröhrchen, einer Mikro-Pipette oder einem sehr feinen Pinsel auf eine hochkant gelegte, beschichtete (raue) Seite der Folie (bzw. Platte) sparsam aufgetragen. Dies kann, je nach Methode, punktförmig (Abstand von unten: etwa 1,5 cm), oder linienförmig (etwa 1,5 cm parallel zur unteren Kante) geschehen. Die Auftragslinie kann auch mit einem feinen Bleistift gekennzeichnet werden. Dabei sollte die Kieselgelschicht möglichst wenig verletzt werden. Nachdem der Extrakt auf der Folie getrocknet ist (dies kann durch einen Haartrockner beschleunigt werden - mit kaltem Luftstrom), kann dieser Auftrage-Vorgang wiederholt werden. Dies soll etwa 10 bis 15 mal passieren. Ist auf der Folie dann der grüne Punkt (bzw. die Linie) wieder getrocknet, wird die Folie in das mit ein wenig Fließmittel gefüllte Apfelmusglas gestellt, danach wird es geschlossen. Das Glas sollte jetzt nicht mehr oder nur sehr vorsichtig berührt werden, da nun der Fließvorgang beginnt. Sobald die Flüssigkeit bis zum Ende des Blattes gestiegen ist (oder schon früher, je nach gewünschtem Ergebnis) wird es aus dem Glas genommen und auf einigen Blatt Papier getrocknet. Erklärung des FließvorgangsDas Fließmittel wird nach oben hin von der Folienschicht aufgenommen. Dabei trägt es den Blattfarbstoffextrakt mit sich. Die verschiedenen Adsorptionsfähigkeiten der einzelnen Bestandteile des Blattes sorgen dafür, dass sich das Gemisch in seine Bestandteile aufgliedert. Dank dieser Methode kann man feststellen, aus welchen Komponenten die Blattfarbstoffe bestehen (siehe linke Abbildung).
Galerie: Der Versuch in 7 BildernLiteratur
|
| Dieser Artikel basiert auf dem Artikel Dünnschichtchromatografie aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. |





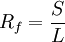 . Die
. Die 

