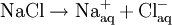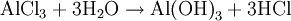Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
HydratisierungUnter Hydratisierung – häufig auch mit Hydratation oder Hydration bezeichnet – versteht man
Weiteres empfehlenswertes FachwissenAnlagerung von Wassermolekülen an Ionen in LösungDie bei der Hydratisierung entstehenden Produkte heißen Hydrate. In anderen Lösungsmitteln, z.B. Ammoniak, treten ähnliche Effekte auf, die allgemein Solvatisierung genannt werden. Die Hydratisierung erfolgt aufgrund der elektrostatischen Kräfte zwischen den geladenen Ionen und den Wasser-Dipolen (Ion-Dipol-Wechselwirkung). Unter Ausbildung von Wasserstoffbrücken zu der ersten Hydrathülle können sich weitere Wassermoleküle anlagern und so eine weitere Hydrat-Sphäre bilden. Als Maß für die Neigung der Ionen, sich mit Wassermolekülen zu verbinden, dient die Hydrationsenergie. Dies ist die Energie, die erforderlich ist um die Ionen aus der wässrigen Lösung in das Vakuum zu bringen. Die Anzahl der gebundenen Wassermoleküle und die Stärke der Bindung hängen von der Größe und der Ladung der Ionen ab. Bei gleicher Ladung bauen die kleineren Ionen eine größere Hydrathülle auf als die größeren. Durch ein "aq" am Ion markiert man, dass das Ion hydratisiert vorliegt: Bei kleinen und/oder mehrfach geladenen Kationen können die gebundenen Wassermoleküle Protonen abgeben, man spricht von Kationsäuren (siehe Lewis-Säuren). Aus Lösungen, die Kationsäuren enthalten, kann das Lösungsmittel Wasser unter Umständen nicht entfernt werden: Anionen sind im Allgemeinen wesentlich größer als Kationen und damit auch schwächer hydratisiert. Anlagerung von Wasser an eine C=C Doppelbindung (Reaktion)Diese Reaktion wird üblicherweise in stark saurer wässriger Lösung durchgeführt. Während bei der Hydrolyse die nicht-Wasser Komponente in zwei Bestandteile zerlegt wird, bleibt sie bei der Hydratisierung als ein Molekül erhalten. Die allgemeine Formel der Reaktion ist:
Im ersten Schritt bindet sich das saure Proton an das weniger substituierte Kohlenstoffatom der Doppelbindung gemäß der Markownikow-Regel. Im zweiten Schritt bindet sich ein H2O Molekül an das höher substituierte Kohlenstoffatom. Zu diesem Zeitpunkt hat das Sauerstoffatom drei Bindungen und eine positive Ladung. Das Proton wird dann von einem weiteren Wassermolekül übernommen. In der Laborpraxis liefert diese Reaktion oft ungewollte Nebenprodukte und ist in der hier beschriebenen einfachen Form kaum zur Herstellung eines Alkohols geeignet. Eine Alternative stellt die Oxymercurierung da. Hier als Beispiel die Reaktion von 1-Methylcyclohexen zu 1-Methylcyclohexanol, mit Schwefelsäure als Katalysator. Kategorien: Chemische Bindung | Chemische Reaktion |
| Dieser Artikel basiert auf dem Artikel Hydratisierung aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. |