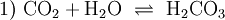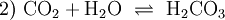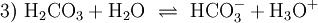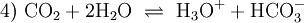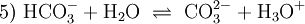Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Kohlensäure
Kohlensäure (H2CO3) ist eine Säure und das Reaktionsprodukt von Kohlenstoffdioxid (CO2) mit Wasser. Die Salze der zweiprotonigen Säure heißen Carbonate bzw. Hydrogencarbonate, auch ihre Ester werden Carbonate genannt. Technische Bedeutung haben die Polyester, die als Polycarbonate bezeichnet werden. Das Gas CO2 ist im Vergleich zu O2 und N2 relativ gut löslich in Wasser und reagiert zu einem geringen Anteil (etwa 0,2 %, je nach Temperatur) zu Kohlensäure: CO2 als Gas wird umgangssprachlich oft fälschlicherweise als Kohlensäure bezeichnet. In der Wasserchemie wird gelöstes CO2 mit der eigentlichen Säure H2CO3 üblicherweise als „freie Kohlensäure“ zusammengefasst. Kohlensäure spielt eine wichtige Rolle im Säure-Basen-Haushalt des Blutes. Weiteres empfehlenswertes Fachwissen
DissoziationsgleichgewichtGelöstes Kohlendioxid steht in wässriger Lösung im Gleichgewicht mit Kohlensäure: Da Kohlensäure formal eine Verletzung der Erlenmeyer-Regel darstellt, liegt das Gleichgewicht sehr weit auf der Seite des gelösten Gases; der Anteil des Säuremoleküls liegt bei nur rund 0,2 %. In Organismen wird die Reaktion durch das Enzym Carboanhydrase beschleunigt. Die Kohlensäure ist eine zweiprotonige Säure. Sie gibt daher ihre Protonen in zwei Dissoziationsstufen an Wasser oder andere Basen ab: Der pH-Wert der ersten Säurekonstante liegt (mit temperaturabhängigen Abweichungen) eigentlich bei ca. 3,88, vergleichbar mit Essigsäure und Zitronensäure. Da aber der Anteil der Kohlensäure gemäß Gleichung 1) schlecht zu bestimmen ist, werden die Reaktionen 2) und 3) zusammengefasst: und ergeben den (fast immer genannten) Wert von ca. 6,5 für den pKs-Wert. Reaktionsprodukt ist das Hydrogencarbonat-Ion HCO3−. Der pKs-Wert für die zweite Säurekonstante liegt um 10,5. Reaktionsprodukt ist das Carbonat-Ion CO32−. Als Trivialnamen für die Summe aus gelöstem Kohlendioxid und Kohlensäure ist „freie Kohlensäure“ gebräuchlich. Sie steht der Summe von Carbonat und Hydrogencarbonat als „gebundener Kohlensäure“ gegenüber. Die Konzentrationen der drei Kohlensäure-Spezies, also der freien Kohlensäure, des Hydrogencarbonat und des Carbonat sowie der Oxoniumionen stehen mit einander durch das Massenwirkungsgesetz in einem berechenbarem Zusammenhang. Die Konzentration der Hydroniumionen wird durch den pH-Wert ausgedrückt. Bei einem gegebenen pH-Wert ist somit das Mengenverhältnis der Spezies festgelegt: Bei pH 4 liegen mehr als 99 % als freie Kohlensäure vor. Bei einem pH-Wert von 6,5, der also gleich ist dem pKs der ersten Säurekonstante, liegen gleich viel freie Kohlensäure und Hydrogencarbonat vor; der Anteil des Carbonats ist noch weit unter 1 %. Etwa bei pH 8,3 liegt der maximale Anteil an Hydrogencarbonat mit ca. 98 % vor; je knapp 1 % sind freie Kohlensäure bzw. Carbonat. Bei einem pH gleich dem pKs der zweiten Säurekonstante von 10,5 liegen gleiche Mengen Hydrogencarbonat und Carbonat sowie ein verschwindender Anteil an freier Kohlensäure vor. Bei pH 12,5 hat das Carbonat einen Anteil um 99 %, Hydrogencarbonat noch knapp 1 %, freie Kohlensäure noch Spuren. Kohlensäure als ReinsubstanzIm Labor ist es gelungen, Kohlensäure als Reinsubstanz zu gewinnen. Bei tiefen Temperaturen und unter absoluter Abwesenheit von Wasser oder Metallionen (beide katalysieren stark die Zersetzungsreaktion zu Kohlenstoffdioxid und Wasser) kann die Kohlenstoffsäure H2CO3 als wasserklare, farblose Flüssigkeit dargestellt werden.[2] „Aggressive Kohlensäure“ und VerwandteEine weitere Gruppe von Trivialnamen, der nicht chemisch unterschiedliche Spezies, sondern Mengenanteile bezeichnet, stammt aus dem Bereich der Aufbereitung von kalkhaltigem Wasser. Dort unterscheidet man die (Menge der) „zugehörigen“ Kohlensäure von der (Menge der) „überschüssigen“ und der „(kalk-)aggressiven Kohlensäure“. Zugehörige Säure hält im Mengengleichgewicht der Kohlensäurespezies den pH-Wert gerade so niedrig, dass die hiervon abhängige Konzentration des Carbonates multipliziert mit der des Calciums gerade noch nicht das Löslichkeitsprodukt überschreitet. Darüber hinaus vorhandene freie Kohlensäure gilt als überschüssig. Davon wiederum ein Teil könnte weiteren Kalk in Lösung bringen, ist also (kalk-)aggressiv. Auch mit Eisen oder anderen Metallen kann Kohlensäure reagieren und so beispielsweise Leitungsrohre angreifen. Auch diese Reaktionen sind konzentrationsabhängig im Gleichgewicht mit entsprechenden Carbonaten. Deshalb spricht man dann z. B. von „Eisen-aggressiver Kohlensäure“. Bei manchen Anwendergruppen, z. B. in der Fischerei, werden die hier genannten Mengenbegriffe oft so missverstanden, als ob z. B. die „aggressive Kohlensäure“ besonders schädlich wäre, etwa für die Fische. Da aber Fische nicht aus Kalk bestehen, richtet sich die aggressive Kohlensäure nicht in anderer Weise gegen sie als der Rest der Kohlensäure. Für die Atmung der Fische ist vielmehr die gesamte gelöste CO2-Konzentration ausschlaggebend, für eine allfällige sauere Verätzung ausschließlich der pH-Wert des Wassers. Die „zugehörige Ks“ wird dort so missverstanden, als ob sie in besonderer Weise an das Hydrogencarbonat gebunden und deshalb nicht durch Wasserbelüftung auszutreiben oder durch Photosynthese von Algen zu verbrauchen wäre. Tatsächlich steht beiden Vorgängen die gesamte „freie Ks“ zur Verfügung, so dass es zu einer Steigerung des pH-Wertes, dadurch zu einer Verschiebung des Mengengleichgewichts hin zu mehr Carbonat und dadurch schließlich zu einer Überschreitung des Löslichkeitsproduktes des Kalkes, also zu einer Kalkfällung kommt. Derivate der KohlensäureDarüber hinaus sind organische Derivate der Kohlensäure bekannt, so verschiedene Kohlensäureester. Sie sind leicht zugänglich durch die Reaktion von Phosgen mit Alkoholen. Von technischer Bedeutung sind vor allem die Amide der Kohlensäure. Ihre Stammverbindung ist der Harnstoff; als Beispiel seien die Urethane (von Urea, Harnstoff) genannt. Es sind substituierte Ester des Monoamids der Kohlensäure, der Carbaminsäure; diese sind die Stammverbindungen überaus wichtiger Kunststoffe, der Polyurethane. VerwendungKohlensäure wird für unzählige Produktionsprozesse weltweit eingesetzt. Dem Endverbraucher dürfte die Kohlensäure wohl am ehesten aus Erfrischungsgetränken bekannt sein. Johann Jacob Schweppe entwickelte im späten 18. Jahrhundert ein Verfahren, mittels dem sich Wasser mit Kohlensäure versetzen lässt. Des Weiteren ist die Kohlensäure ein wichtiger Bestandteil der sterilen Verpackungstechnik. Im 19.Jahrhundert hat man angefangen, Kohlensäure in Mineralwasser beizumischen, um dieses haltbar zu machen. Literatur
Quellen
Kategorien: Mineralsäure | Carbonat |
|||||||||||||||||||||||||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Kohlensäure aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. | |||||||||||||||||||||||||||||||||||||||||||||||