Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Kubisches KristallsystemDas kubische Kristallsystem oder auch kubisches Gitter ist ein System zur Beschreibung des Kristall-Aufbaus eines Festkörpers. Es weist unter den sieben Kristallsystemen die höchste Symmetrie auf. Das Koordinatensystem ist rechtwinklig, die Achsen sind alle gleich lang, d. h. vertauschbar. Die Symmetrieelemente, welches das Kristallsystem definieren, sind vier dreizählige Achsen durch die Raumdiagonalen und zweizählige Drehachsen durch die Würfelflächen. Die drei zugehörigen kubischen Raumgitter oder Bravais-Gitter sind das primitiv-kubische, das kubisch-flächenzentrierte (fcc: face-centered cubic) und das kubisch-raumzentrierte Gitter (bcc: body-centered cubic). Beispiele für Minerale, die in kubischen Systemen kristallisieren, sind Diamant, Fluorit, Minerale der Granatgruppe, Halit, Galenit (Bleiglanz), Pyrit und Spinell. Weiteres empfehlenswertes Fachwissen
EigenschaftenUm ein Körper des kubischen Kristallsystems zu sein, muss dieser Körper folgende Eigenschaften haben:
KristallklassenDas kubische Kristallsystem beinhaltet fünf Kristallklassen, die je nach verwendetem Symbolsystem der Kristallographie mit unterschiedlichen Kurzzeichen bezeichnet werden:
SymmetrienKubische Gitter besitzen zahlreiche Symmetrien, unter anderem:
Weil das Gitter nur aus mathematischen Punkten besteht, hat das Gitter sehr häufig eine höhere Symmetrie als die Kristallstruktur, die aus Atomen, Molekülen oder Ionen aufgebaut ist. Körper im kubischen KristallsystemDabei unterscheidet man zwischen: charakteristischen Formen des kubischen Kristallsystems
Flächenformen des kubischen Kristallsystems
Ebenfalls kubische Kristallformen sind Mischformen aus den oben angegebenen Flächenformen. Bravais-Gitter im kubischen KristallsystemFür die Beschreibung der Kristallstruktur eines kristallinen Stoffes wird zusätzlich zum Kristallsystem die Zentrierung der Elementarzelle, die alle für die Beschreibung der Struktur notwendigen Atome, Ionen oder Moleküle enthält, in Form des Bravais-Gitters angegeben. Das kubische Kristallsystem umfasst folgende Bravais-Gitter: Kubisch-primitives GitterBei einer kubisch primitiven Struktur (auch sc für simple cubic) befindet sich jeweils an den Ecken der würfelförmigen Elementarzelle ein Atom. Die Raumerfüllung beträgt bei gleich großen, sich berührenden Kugeln auf den Gitterplätzen ca. 52 %. Beispiele für eine kubisch primitive Kristallstruktur sind unter anderem α-Polonium, sowie die Hochdruckmodifikationen von Phosphor und Antimon. Auch in der chemischen Verbindung Natriumchlorid (NaCl, Kochsalz) lässt sich die kubisch primitive Form wiederfinden, wenn man sie als Ganzes betrachtet. Dabei wechseln sich die Atome in der Besetzung der Elementarwürfelecken allerdings ab. Betrachtet man Natrium und Chlor für sich, bilden sie ein kubisch flächenzentriertes Kristallgitter. Kubisch-raumzentriertes GitterIm kubisch raumzentrierten Kristallgitter (krz, auch bcc für body centered cubic) besitzt jede Kugel statt zwölf Nachbarn, wie in einer dichtesten Kugelpackung, nur acht nächste Nachbarn. Der Raumfüllungsgrad dieser Packung beträgt 68 Prozent und somit nur 92 Prozent der einer dichtesten Kugelpackung. Die größte Gitterlücke ist die Tetraederlücke. Eine kubisch raumzentrierte Kristallstruktur haben unter anderem α-Eisen, Caesium, Chrom, Kalium, Molybdän, Niob, Rubidium, Tantal, Vanadium und Wolfram. Nach dem Wolfram wird dieser Strukturtyp auch Wolframtyp genannt. Das Atomium in Brüssel soll eine 165-milliardenfache Vergrößerung der kubisch-raumzentrierten Elementarzelle des Eisens darstellen. Kubisch-flächenzentriertes GitterBeim kubisch flächenzentrierten Kristallgitter (kfz, auch fcc für face centered cubic; ebenfalls "kubisch dichteste Packung"="ccp"="cubic closed package" genannt) sind acht Atome so angeordnet, dass sie die Ecken eines Würfels bilden. Zusätzlich sind insgesamt sechs weitere Atome mittig auf den Würfelflächen so angeordnet, dass bei Verbindung dieser ein Oktaeder entsteht. In diesem Gitter ist die Raumfüllung ca. 74 Prozent, entsprechend einer dichtesten Kugelpackung. Das bekannteste Beispiel einer kubisch flächenzentrierten Kristallstruktur ist das Kochsalz (siehe auch Natriumchlorid-Struktur). Die kleineren Na+-Ionen befinden sich dann in den Oktaederlücken des fcc-Gitters aus Cl--Ionen. Dabei ist jedes Na+-Ion oktaedrisch von sechs Cl--Ionen umgeben und umgekehrt. Der Natriumchlorid-Strukturtyp kommt bei vielen anorganischen Salzen vor (z. B. MgO, CaO, MgS, LiCl, NaH, AgCl, usw.). Eine kubisch flächenzentrierte Kristallstruktur haben bei den Metallen z. B. Aluminium, Blei, γ-Eisen, Gold, Calcium, Strontium, Cer, Iridium, Kupfer, Nickel, Palladium, Platin, Rhodium und Silber. Nach dem Kupfer wird diese Struktur auch Kupfer-typ genannt. Auch die Kristallstruktur des Diamants hat ein kubisch flächenzentriertes Gitter mit einer Basis von zwei identischen Atomen bei [000] und Siehe auch
Kategorien: Kubisches Kristallsystem | Kristallographie |
|||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Kubisches_Kristallsystem aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. |





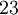
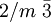
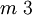
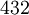
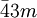
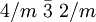
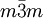
![\left[{1 \over 4} {1 \over 4} {1 \over 4}\right]](images/math/4/2/3/423b34f78a7477a9cf0ff90b021712ca.png) .
. 

