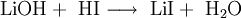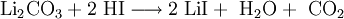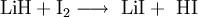Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Lithiumiodid
Lithiumiodid LiI, das Lithiumsalz der Iodwasserstoffsäure, bildet farblose, stark hygroskopische Kristalle mit einem Schmelzpunkt von 469°C, einem Siedepunkt von 1180°C und einer Dichte von 4,1 g·cm-3. Die molare Masse des wasserfeien Lithiumiodids beträgt 133,85 g/mol. An Luft färben sich die Kristalle schnell gelblich bis bräunlich, da das Iodid zum Iod oxidiert wird. Neben dem wasserfreien Lithiumiodid existieren noch verschiedene Hydrate, bekannt sind LiI·nH2O mit n= 0,5, 1, 2 und 3. Weiteres empfehlenswertes Fachwissen
HerstellungDie Herstellung von Lithiumiodid erfolgt durch Umsetzung wässriger Lithiumhydroxid- oder Lithiumcarbonatlösungen mit Iodwasserstoff und anschließender Aufkonzentrierung und Trocknung. Das wasserfreie Lithiumiodid kann auch durch Reaktion von Lithiumhydrid mit Iod in wasserfreiem Diethylether hergestellt werden. EigenschaftenDas Trihydrat weist einen Schmelzpunkt von 72°C und eine Dichte von 3,5 g·cm-3 auf. Beim Erhitzen verliert es bei 80°C zwei Moleküle Kristallwasser und bei 300°C ein Molekül Kristallwasser. Lithiumiodid ist gut in Wasser löslich (> 500g LiI/l Wasser). VerwendungDas wasserfreie Lithiumiodid wird für organische Synthesen verwendet, in Batterien dient es als Elektrolyt. Dotierte Kristalle dienen als Szintillationsdetektor für energiereiche Neutronen. QuellenKategorien: Giftiger Stoff | Lithiumverbindung | Iodid |
|||||||||||||||||||||||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Lithiumiodid aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. | |||||||||||||||||||||||||||||||||||||||||||||