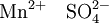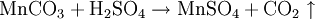Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Mangan(II)-sulfat
Mangan(II)-sulfat ist das zweiwertige Mangansalz der Schwefelsäure mit der Summenformel MnSO4. Mangan(II)-sulfat bildet im kristallwasserhaltigen Zustand blassrosa monokline, im wasserfreien Zustand weiße Kristalle. Weiteres empfehlenswertes Fachwissen
VorkommenIn der Natur kommt Mangan(II)-sulfat als das Mineral Mallardit vor (MnSO4 · 7 H2O). Gewinnung und DarstellungMangan(II)-sulfat kann durch Auflösen von Mangan(II)-carbonat in Schwefelsäure dargestellt werden.
EigenschaftenMangan(II)-sulfat ist gut löslich in Wasser, aber unlöslich in Alkoholen. Es bildet mehrere Hydrate (Monohydrat, Tetrahydrat, Heptahydrat). Die wasserfreie Substanz erhält man durch Abrauchen der meisten Manganverbindungen mit Schwefelsäure. VerwendungMangan(II)-sulfat findet Verwendung in der Zeugdruckerei, Porzellanfabrikation, zur Desinfektion, in der Färberei und in der Holzbeize. Kategorien: Gesundheitsschädlicher Stoff | Umweltgefährlicher Stoff | Manganverbindung | Sulfat |
||||||||||||||||||||||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Mangan(II)-sulfat aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. | ||||||||||||||||||||||||||||||||||||||||||||