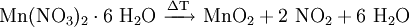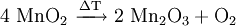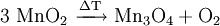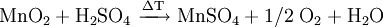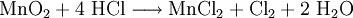Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Mangandioxid
Weiteres empfehlenswertes Fachwissen
GeschichteMangandioxid (Braunstein) wurde früher unter Handwerkern als „Glasmacherseife“ bezeichnet, da es durch Eisen(III)-silikate verfärbte Glasschmelzen entfärben konnte. Schon in den Gläsern der alten Ägypter und Römer findet man etwa 2 % Manganoxide. Wahrscheinlich wurde schon zu dieser Zeit Braunstein zum Aufhellen der Gläser benutzt. VorkommenMangandioxid findet man als rhombisch kristallisierter Pyrolusit (Weichmanganerz) und tetragonal kristallisierter Polianit in großem Umfang im Südural und in Südafrika. Zusammen mit anderen Eisenverbindungen ist es oft ein Hauptbestandteil der Umbraerden und anderer brauner, dunkelfarbiger Erden. Gewinnung und DarstellungMangandioxid wird durch Mahlen von Pyrolusit oder durch das Erhitzen von Mangan(II)-nitrat an der Luft auf über 500 °C hergestellt. Heute jedoch wird Mangandioxid hauptsächlich durch Elektrolyse einer Lösung von Mangan(II)-sulfat gewonnen. Zweiwertige Mangan-Ionen (Mn2+) oxidieren an der Anode zu dreiwertigen Mn3+-Ionen, die anschließend zu Mn2+- und Mn4+-Ionen (disproportionieren). Dabei lagert sich Braunstein an der Anode ab. EigenschaftenMangandioxid ist ein braunschwarzes Pulver, das in Wasser unlöslich ist. Außerdem findet keine Reaktion mit kalter Schwefel- oder Salpetersäure statt. ReaktionenDurch Erhitzen über 450 °C wird unter Sauerstoffabgabe Mangan(III)-oxid ( Mn2O3) gebildet. Durch Erhitzen über 600 °C wird unter Sauerstoffabgabe Mangan(II, III)-oxid (Mn3O4) gebildet; Mn3O4 enthält 72 % Mangan. Das Erhitzen unter Zusatz von Schwefelsäure führt zur Abspaltung von Sauerstoff unter Bildung von Mangan(II)-sulfat. Wasserstoffperoxid zersetzt sich in Anwesenheit von Mangandioxid unter Sauerstoffabgabe. Das Mangandioxid wirkt dabei als Katalysator. Mit Salzsäure reagiert Mangandioxid unter Chlorentwicklung zu Mangan(II)-chlorid. VerwendungMangandioxid wird vielfältig als Oxidationsmittel in organischen Synthesen eingesetzt:
Kategorien: Gesundheitsschädlicher Stoff | Manganverbindung | Oxid |
|||||||||||||||||||||||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Mangandioxid aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. | |||||||||||||||||||||||||||||||||||||||||||||