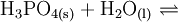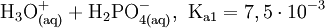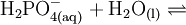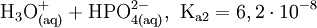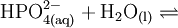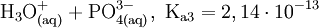Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Phosphorsäure
Die normale oder ortho-Phosphorsäure ist die wichtigste Säure des Phosphors. Die wasserfreie Substanz ist stark hygroskopisch. Sie ist eine dreiprotonige Säure und reagiert bezüglich der ersten Deprotonierung als mittelstarke Säure. Von ihr leiten sich die Kondensate Diphosphorsäure, Meta- und Polyphosphorsäuren ab. Als Lebensmittelzusatzstoff wird Phosphorsäure als E 338 deklariert. Weiteres empfehlenswertes Fachwissen
Gewinnung und DarstellungPhosphorsäure kann aus Rohphosphat (meistens Apatit, Ca5(PO4)3(F, OH, Cl)) mit Schwefelsäure, Salzsäure oder Salpetersäure hergestellt werden. Als Nebenprodukte fallen dabei CaSO4 (Anhydrit, Gips) und H2[SiF6] (Hexafluorokieselsäure) an. Alternativ lässt sich Phosphorsäure durch Verbrennung elementaren Phosphors zu Phosphorpentoxid, P4O10, und anschließende Hydrolyse herstellen (sogenannte thermische Phosphorsäure). EigenschaftenDie Phosphorsäure ist eine dreiwertige Säure, die ihren Wasserstoff als solvatisierte Protonen in drei Stufen unter Bildung von Dihydrogenphosphat-, Hydrogenphosphat- und Phosphat-Anionen abgeben kann. Die zugehörigen pKs-Werte betragen pKs1 = 2,161; pKs2 = 7,207 und pKs3 = 12,325[1]. VerwendungPhosphorsäure dient als Ausgangsstoff zur Herstellung phosphathaltiger Dünger (in den USA >90 % der Produktion), von Waschmitteln, Rostentfernern bzw. von Rostumwandler sowie zur Passivierung von Eisen und Zink zum Schutz vor Korrosion. In der Zahnmedizin findet Zinkphosphatzement Verwendung. Während sie in hoher Konzentration ätzend wirkt, wird sie verdünnt in der Lebensmittelindustrie als Konservierungsmittel, Säuerungsmittel (vor allem in Cola-Getränken) sowie als Säureregulator eingesetzt (E 338), denn die Phosphorsäure ist bis auf ihre ätzende Wirkung für den menschlichen Organismus ungiftig. Sie eignet sich auch zur Herstellung von Pufferlösungen (verschiedene „Phosphatpuffer“). Biologische BedeutungPhosphorsäureester spielen im Stoffwechsel eine zentrale Rolle, insbesondere als Energie- und Gruppenüberträger (siehe z. B. ATP bzw. GTP). Sie sind integraler Bestandteil der DNA, der RNA, vieler Coenzyme etc. NachweisDie Phosphorsäure und lösliche Phosphate lassen sich durch Fällung mit Ammoniummolybdat zu gelbem Ammoniummolybdatophosphat, oder durch Fällung mit Magnesiumionen in ammoniakalischer Lösung zu MgNH4PO4 nachweisen. Quellen
Siehe auchKategorien: Ätzender Stoff | Mineralsäure | Phosphorverbindung | Phosphat |
|||||||||||||||||||||||||||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Phosphorsäure aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. | |||||||||||||||||||||||||||||||||||||||||||||||||