Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
PolymerisationDie Polymerisation ist eine chemische Reaktion, bei der Monomere, meist ungesättigte organische Verbindungen, unter Einfluss von Katalysatoren und unter Auflösung der Mehrfachbindung zu Polymeren (Moleküle mit langen Ketten, bestehend aus miteinander verbundenen Monomeren) reagieren. Dabei unterscheidet man zwischen Homo-Polymerisation, bei der nur eine Monomerart umgesetzt wird, und Co-Polymerisation, bei der zwei oder mehr verschiedene Monomere zur Reaktion gebracht werden. Die Produkte der Polymerisation nennt man Polymerisate. Weiteres empfehlenswertes Fachwissen
Historische Informationen1907 gelang dem Chemiker Adolf von Baeyer (1835 – 1917) erstmals die Polykondensation von Phenol und Formaldehyd zum so genannten Bakelit. Damit legte er die Grundlage für die heutige Polymerchemie. Hermann Staudinger, der sich hauptsächlich mit der Polymerchemie befasste, erklärte in Thesen die Polymerisation schließlich als Kettenreaktion, bei der Makromoleküle entstehen. MechanismenBei den Polyreaktionen werden zwei Klassen unterschieden: Stufenwachstumsreaktionen und Kettenwachstumsreaktionen. Während im ersten Fall auch bereits vorhandene Kettensegmente zu einer größeren Kette zusammenwachsen können (z. B. bei der Polyaddition und Polykondensation), lagert sich im zweiten Fall immer ein Molekül nach dem anderen an das sogenannte reaktive Kettenende an. Zu den Kettenwachstumsreaktionen gehören die radikalische Polymerisation, ionische Polymerisation und Koordinationspolymerisation (s. u.), die unter Verwendung von Ziegler-Natta-Katalysatoren durchgeführt wird. Thermische PolymerisationDie thermische Polymerisation ist eine spezielle Form der radikalischen Polymerisation, die sich auf den Reaktionsstart bezieht. Bei ihr wird bis zur Bildung von Radikalen Wärme zugeführt, die so die Polymerisation starten (s.u.). Radikalische PolymerisationDie radikalische Polymerisation umfasst im Wesentlichen drei Teilschritte: 1. Startreaktion, bei der das aktive Zentrum gebildet wird. 2. Wachstumsreaktion, bei der die makromolekulare Kette in einer Kettenreaktion wächst (wiederholte Anlagerung der Monomere) und 3. Abbruchreaktion, bei der das Wachstum der Kette durch Disproportionierungsreaktionen oder Kombinierung irreversibel beendet wird. ReaktionenZum Kettenstart bricht ein Radikal die Mehrfachbindung (beispielsweise eine C=C-Doppelbindung einer Vinylgruppe) auf und erzeugt ein wachstumsfähiges Primärradikal, an das sich nun in einer Wachstumsreaktion mit geringer Aktivierungsenergie ständig Monomere anlagern. Durch das Zusammentreffen zweier Radikale oder durch Disproportionierung wird ein Kettenabbruch hervorgerufen. Um die Reaktion gezielt zu stoppen, können spezielle Reagenzien, so genannte Radikalfänger, zugegeben werden. Daneben kann eine gewisse Kontrolle über die molare Masse erreicht werden, in dem man sog. Kettenüberträger der Polymerisation hinzufügt. Kinetik der radikalischen PolymerisationFür jede der Teilreaktionen der radikalischen Polymerisation lassen sich Gleichungen für die Reaktionsgeschwindigkeiten formulieren. Die Kenntnis dieser Zusammenhänge ermöglicht es, den mittleren Polymerisationsgrad eines entstehenden Polymers zu steuern, sowie einige bei der Polymerisation auftretende Effekte zu deuten.
Die Geschwindigkeit vini der Initiation hängt von der Konzentration des Initiators [I] und von dem entsprechenden Geschwindigkeitskoeffizienten kini ab:
Die Geschwindigkeit vw des Kettenwachstums, also des Monomerverbrauchs, ist abhängig von der Monomerkonzentration [M], der Konzentration der Polymerradikale [P * ] und dem entsprechenden Geschwindigkeitskoeffizienten kw:
Die Geschwindigkeit vstop der Rekombination, also des Verbrauchs an Polymerradikalen P*, hängt quadratisch von deren Konzentration [P * ] ab und natürlich vom Koeffizienten kstop:
Die Geschwindigkeit der Übertragung vtrans, hängt von der Konzentration des Überträgers [Trans], der Konzentration der Polymerradikale [P * ] und dem Koeffizienten ktrans ab:
Aus den gegebenen Geschwindigkeitsgesetzen kann man eine Formel für die Wachstumsgeschwindigkeit herleiten. Diese gilt nur bei mittleren Umsätzen, gibt aber dann im Grunde die Bruttoreaktionsgeschwindigkeit an:
Ebenso kann man das Zahlenmittel des Polymerisationsgrades
PolymerisationsverlaufDer Reaktionsablauf der radikalischen Polymerisation sieht wie folgt aus:
Es entstehen zunehmend Initiator-Radikale, Primärradikale und wenige oligomere Radikale. Die Gesamtreaktionsgeschwindigkeit steigt rasant, der durchschnittliche Polymerisationsgrad ist gering.
Bei so geringem Umsatz kann die Monomerkonzentration als konstant betrachtet werden, ebenso die Anzahl vorhandener Radikale, die Gesamtreaktionsgeschwindigkeit bleibt konstant, während der Polymerisationsgrad steigt. Es entstehen erste Makroradikale. Die Polymerisationsgradverteilung ist relativ eng.
Die Monomerkonzentration nimmt durch den Verbrauch stark ab, wodurch die Reaktionsgeschwindigkeit abnimmt. Es sind nun viele Makroradikale vorhanden und Abbruch-Reaktionen finden statt.
Die Polymerisation unterliegt einer Selbstbeschleunigung. Es liegen nun sehr große Polymerradikale vor, die wegen ihrer Größe diffusionsgehindert sind. Das hat zur Folge, dass immer weniger Abbruchreaktionen stattfinden, während der Initiator weiterhin zerfällt und neue Radikale bildet. In dieser Phase nimmt der Polymerisationsgrad stark zu, und die Polymerisationsgradverteilung wird sehr breit.
Die Reaktionsgeschwindigkeit fällt zunehmend bis zum Minimum ab. Die Polymermoleküle und Polymerradikale sind mittlerweile so groß und unbeweglich, dass das Reaktionsgemisch langsam erstarrt (deswegen "Glas"). Es wird nie der thermodynamisch mögliche maximale Umsatz erreicht, da viele Monomere im erstarrten Reaktionsgemisch gefangen bleiben, ohne zu reagieren. Aktuelle TrendsSeit wenigen Jahren ist es möglich, über die radikalische Polymerisation Kontrolle zu erlangen. Mit den Techniken der Controlled Free Radical Polymerization (LFRP) gelingt es, Polymere mit enger Molmassenverteilung durch Zusatz eines 'Kontrollreagenz' zu synthetisieren. Je nach Verwendung des Kontrollreagenzes unterscheidet man bisher zwischen Atom Transfer Radical Polymerization (ATRP), Nitroxide Mediated Polymerization (NMP) und Kettentransfermethoden wie dem Reversible Addition-Fragmentation Chain Transfer-Prozesses (RAFT). Kationische und Anionische PolymerisationHier greift, im Unterschied zur radikalischen Polymerisation, ein Kation bzw. Anion die Mehrfachbindung an, um den Kettenstart hervor zu rufen. Der Kettenabbruch erfolgt durch Zusammentreffen von Kation und Anion.
KoordinationspolymerisationDie Katalysatoren sind Übergangsmetallverbindungen, deren Struktur so zu charakterisieren ist, dass ein Zentralatom (das Metall-Ion) derart von Liganden umgeben ist, dass ein Monomer und die Polymerkette daran anlagern (koordinieren) können. Das Prinzip beruht auf einer Aktivierung der Monomere aufgrund der Wechselwirkung des Monomers mit dem Metall. Die Doppelbindung im Monomer wird hierdurch geschwächt und die Anlagerung eines zweiten Monomers initiiert. Zur Stabilisierung der so entstandenen Komplexverbindung schiebt sich das Monomer in die bereits vorhandene Polymerkette ein und ein weiteres Monomer wird angelagert usw. Die Polymerisationsreaktion wird so in die Wege geleitet. Das Verfahren wird auch Insertionspolymerisation genannt. Der Vorteil der Koordinationspolymerisation liegt darin, dass je nach Wahl von Katalysator und Monomeren die Taktizität des entstehenden Polymers gesteuert werden kann, die wesentlichen Einfluss auf die Polymereigenschaft haben kann. Es gibt verschiedene Arten von Koordinationspolymerisationen mit unterschiedlichen Mechanismen. Die wichtigste ist die nach ihren Entdeckern benannte Ziegler-Natta-Polymerisation, die es erlaubt, bei niedrigen Temperaturen und niedrigen Drücken zum Beispiel Ethen zu linearem Polyethylen hoher Dichte (PE-HD) umzusetzen. Von großer Bedeutung ist zudem die Polymerisation mit Metallocen-Katalysatoren. Speziellere Arten der Koordinationspolymerisation wie die oben erwähnte ringöffnende Metathesepolymerisation (Ring-Opening Metathesis Polymerization, ROMP) finden ihre Anwendung bei der Herstellung von Spezialpolymeren, die mittels Ringöffnung und Verknüpfung cyclischer Monomere durch Übergangsmetallkatalysatoren produziert werden. Technische VerfahrenPolymerisation
PolykondensationPolykondensation ist die chemische Verknüpfung von Monomeren unter Abspaltung von Wasser oder anderen kleinen Molekülen unter Ausbildung eines Polymers. Durch das Freisetzen dieser Nebenprodukte (Wasser, Ammoniak, Alkohole, Chlorwasserstoff usw.) müssen diese kontinuierlich abgeführt werden. Ansonsten stoppt die Reaktion bei sehr niedrigen molaren Massen gemäß dem Prinzip von Le Chatelier. Die erste Polykondensation gelang 1872 dem deutschen Chemiker Adolf von Baeyer. Er beschrieb die Reaktion von Phenol und Formaldehyd zu Bakelit. Für Details siehe den Artikel Polykondensationsreaktion. Literatur
Kategorien: Makromolekulare Chemie | Chemische Reaktion |
|
| Dieser Artikel basiert auf dem Artikel Polymerisation aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. |





![v_{\text{ini}}= - \frac {\mathrm{d}[I]} {\mathrm{d}t} = k_{\text{ini}} \cdot [I]](images/math/0/1/4/014e1bf6c64c0990bab906647d4a663e.png)
![\frac {\mathrm{d}[R*]} {\mathrm{d}t} = 2f \cdot k_{ini} \cdot [I]](images/math/b/8/3/b83cdbbe9e8430606ec12d9f66b89145.png)
![v_{w}= - \frac {\mathrm{d}[M]} {\mathrm{d}t} = k_{w} \cdot [M] \cdot [P*]](images/math/c/d/f/cdff58ddd20825fb1f7ab7760a735120.png)
![v_{stop}= - \frac {\mathrm{d}[P*]} {\mathrm{d}t} = k_{\text{stop}} \cdot [P*]^{2}](images/math/a/a/1/aa18ef22b9b80be43d411da01310d260.png)
![v_{\text{trans}}= k_{\text{trans}} \cdot [P*] \cdot [Trans]](images/math/f/d/9/fd97221561e1240a0bc712452cc482c7.png)
![v_{w}= k_{w} \cdot \sqrt {2f \cdot \frac {k_{ini}} {k_{stop}}} \cdot [M] \cdot \sqrt {[I]}](images/math/2/4/e/24e2faaa16540bf75df301d2baafbe27.png)
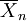 bestimmen. Es ergibt sich aus dem Verhältnis der Wachstumsgeschwindigkeit zu den Geschwindigkeiten aller Reaktionen, bei denen das Wachstum abbricht:
bestimmen. Es ergibt sich aus dem Verhältnis der Wachstumsgeschwindigkeit zu den Geschwindigkeiten aller Reaktionen, bei denen das Wachstum abbricht:
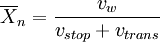
![\frac {1} {\overline {X}_n} = \frac {1} {\overline {X}_{n,0}} + \frac {k_{trans}} {k_w} \cdot \frac {[Trans]} {[M]} = \frac {1} {\overline {X}_{n,0}} + C \cdot \frac {[Trans]} {[M]}](images/math/4/9/e/49e87f1c67248a0e8b4313c93e03fa2b.png)
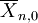 das Zahlenmittel des Polymerisationsgrades bei Abwesenheit eines Überträgers.
das Zahlenmittel des Polymerisationsgrades bei Abwesenheit eines Überträgers.


