Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
RingprobeAls Ringprobe bezeichnet man eine chemische Reaktion zum qualitativen Nachweis von Nitrat-Ionen in wässrigen Lösungen. Dazu wird die Probelösung in einem Reagenzglas mit einigen Tropfen Eisen(II)-sulfat-Lösung versetzt und anschließend vorsichtig mit konzentrierter Schwefelsäure unterschichtet. An der Schichtgrenze von Probelösung und Schwefelsäure findet eine Redoxreaktion statt: Nitrat-Ionen werden zu Stickstoffmonoxid reduziert und die Eisen(II)-Ionen (Fe2+) zu Eisen(III)-Ionen (Fe3+) oxidiert: Weiteres empfehlenswertes FachwissenIm weiteren Reaktionsverlauf lagert sich Stickstoffmonoxid an überschüssige, mit Wasser komplexierte Eisen(II)-Ionen an. Der dabei gebildete Pentaaquanitrosyleisen(II)-Komplex führt zu einer ringförmigen Braunfärbung (je nach Konzentration kann diese auch bis auf ein fahles Violett verringert sein, es ist daher eine Negativprobe zum Vergleich sehr hilfreich) entlang des Rands des Reagenzglases, die namensgebend für die Nachweisreaktion ist: Nitrit-Ionen stören diesen Nachweis, da sich die Lösung bereits bei der Zugabe der Eisen(II)-Lösung braun färbt. Durch Kochen mit Harnstoff werden anwesende Nitrit-Ionen beseitigt. Nitrit-Ionen können mit Lunges-Reagenz qualitativ nachgewiesen werden. Es kann auch zu Konzentrationsniederschlag entlang der Schichtgrenze kommen. Diese ist meist weiß und lässt subtil positive Ergebnisse nicht mehr erkennen. |
| Dieser Artikel basiert auf dem Artikel Ringprobe aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. |


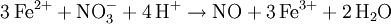



![\mathrm{[Fe(H_2O)_6]^{2+} + NO \rightarrow [Fe(H_2O)_5NO]^{2+} + H_2O} \!](images/math/6/7/0/67072c6da3b93d592d9aaa50b6c05df6.png)


