Wie sich ein Kristall in Wasser löst
Der Lösungsvorgang ist für die Chemie von fundamentaler Bedeutung – aber sehr schwer zu beobachten
Wie sich ein Molekül aus einem festen Kristallverband in einem flüssigen Lösemittel löst, haben Chemiker der Ruhr-Universität Bochum erstmals auf molekularer Ebene beobachtet. Bei Raumtemperatur erfolgt der Prozess zu schnell, um ihn entschlüsseln zu können. Daher nutzte das Team des Exzellenzclusters Ruhr Explores Solvation, kurz Resolv, mikroskopische Methoden, die mit besonders tiefen Temperaturen arbeiten. Die relevanten Schritte des Lösevorgangs beschreibt die Gruppe um Dr. Karsten Lucht und Prof. Dr. Karina Morgenstern vom Lehrstuhl für Physikalische Chemie I in der Zeitschrift „Angewandte Chemie“ vom 11. Oktober 2018.

Karina Morgenstern und Karsten Lucht mit dem Versuchsaufbau an der Ruhr-Universität
© RUB, Marquard
„Den Löseprozess zu verstehen ist von grundlegender Bedeutung für die Chemie, da das Wissen helfen könnte, die Wechselwirkung zwischen Lösemittel und gelösten Molekülen gezielt zu beeinflussen und damit chemische Reaktionen noch umfassender zu kontrollieren“, erklärt Karsten Lucht.
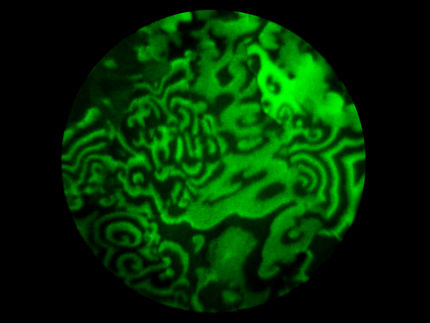
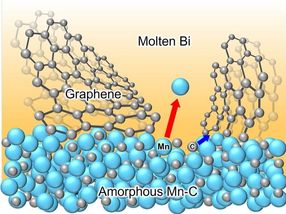
Für die Studie analysierten die Chemiker Kristalle eines organischen Moleküls mit der Tieftemperatur-Rastertunnelmikroskopie, die bei minus 265 Grad Celsius arbeitet. Bei dieser Temperatur kommen molekulare Bewegungen zum Stillstand, sodass die einzelnen Moleküle abgebildet werden können.
Wasser löst Kristallverband auf
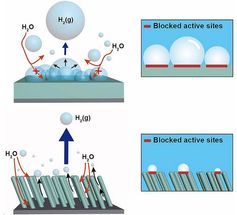
Die Forscher fixierten die organischen Moleküle auf einer speziellen Silberoberfläche. Darauf bildeten die funktionellen Gruppen der Moleküle Ketten. „Diese Struktur entspricht einem eindimensionalen Kristall“, erklärt Lucht. Dann gaben die Wissenschaftler eine geringe Menge Wasser hinzu, das sich an definierten Positionen an die organischen Moleküle anlagerte. Schließlich erwärmten sie das System auf minus 193 Grad Celsius, wobei die Kristallstruktur komplett verloren ging.
„Der Verlust der molekularen Ordnung entspricht dem Auflösen des organischen Kristalls in einer realen Lösung“, beschreibt Karina Morgenstern. Die einzelnen organischen Moleküle wechselwirken nur noch mit den Wassermolekülen und können daher als gelöst aufgefasst werden. „So konnten wir die relevanten Schritte des Lösevorgangs erstmals an einzelnen Molekülen beobachten, also den trockenen Kristall, die Anlagerung des Lösemittels an ihn und seine vollständige Auflösung“, resümiert die Forscherin.
Originalveröffentlichung
Weitere News aus dem Ressort Wissenschaft

Holen Sie sich die Chemie-Branche in Ihren Posteingang
Ab sofort nichts mehr verpassen: Unser Newsletter für die chemische Industrie, Analytik, Labor und Prozess bringt Sie jeden Dienstag und Donnerstag auf den neuesten Stand. Aktuelle Branchen-News, Produkt-Highlights und Innovationen - kompakt und verständlich in Ihrem Posteingang. Von uns recherchiert, damit Sie es nicht tun müssen.