Nachhaltige "Nano-Himbeere" zur Neutralisierung von giftigem Kohlenmonoxid
Wissenschaftler des Nagoya Institute of Technology (NITech) in Japan haben eine nachhaltige Methode entwickelt, um Kohlenmonoxid, das geruchlose Gift, das von Autos und Heizkesseln produziert wird, zu neutralisieren.
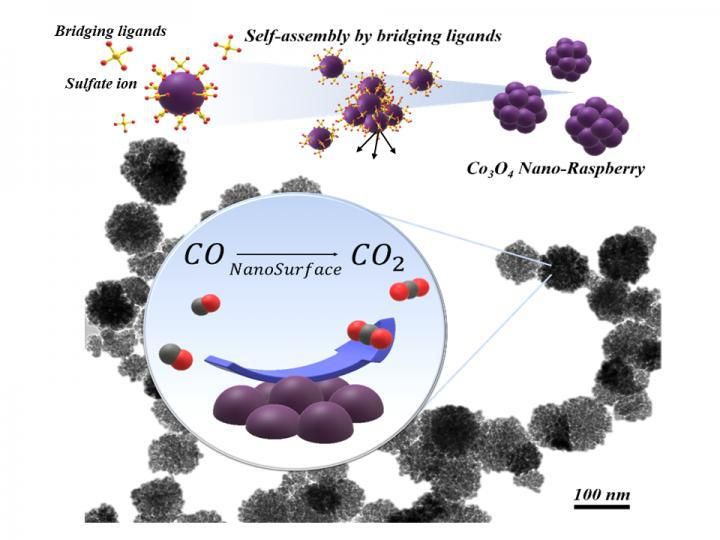
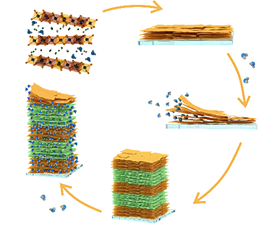
Synthese von Kobaltoxidpartikeln mit komplexen, dreidimensionalen, himbeerförmigen Nanostrukturen durch hydrothermale Behandlung. Natriumsulfate fungierten als Brückenliganden, um die Selbstorganisation zu fördern und das Partikelwachstum zu unterdrücken. Die hochgeordnete und komplexe Oberflächen-Nanostruktur mit einem Durchmesser von 7-8 nm zeigt eine gute Strukturstabilität und hohe Aktivität bei der CO-Oxidationsreaktion.
NITech
Traditionell benötigt Kohlenmonoxid ein Edelmetall - einen seltenen und teuren Bestandteil -, um sich in Kohlendioxid umzuwandeln und sich leicht in der Atmosphäre zu verteilen. Obwohl das Edelmetall die strukturelle Stabilität bei verschiedenen Temperaturen gewährleistet, ist es eine kosteneffiziente und endliche Ressource, und die Forscher waren bestrebt, eine Alternative zu finden.
Nun hat ein Team um Dr. Teruaki Fuchigami am NITech einen himbeerförmigen Nanopartikel entwickelt, der zu dem gleichen Oxidationsprozess fähig ist, der Kohlenmonoxid zu einem zusätzlichen Sauerstoffatom führt und seine höchste toxische Wirkung verliert.
"Wir haben festgestellt, dass die himbeerförmigen Partikel sowohl eine hohe strukturelle Stabilität als auch eine hohe Reaktivität bereits in einer einzigen nanoskaligen Oberflächenstruktur erreichen", sagt Dr. Fuchigami, Assistenzprofessor am Department of Life Science and Applied Chemistry an der NITech und Erstautor auf dem Papier.
Der Schlüssel, so Dr. Fuchigami, ist die Gewährleistung, dass die Partikel hochkomplex, aber organisiert sind. Ein einzelnes, einfaches Partikel kann Kohlenmonoxid oxidieren, aber es verbindet sich natürlich mit anderen einfachen Partikeln. Diese einfachen Partikel verdichten sich und verlieren ihre Oxidationsfähigkeiten, insbesondere wenn die Temperaturen in einem Motor oder Kessel steigen.
Katalytische Nanopartikel mit einfachen nanoskaligen und komplexen dreidimensionalen (3D) Strukturen können sowohl eine hohe strukturelle Stabilität als auch eine hohe katalytische Aktivität erreichen, sind aber mit herkömmlichen Methoden nur schwer herstellbar. Dr. Fuchigami und sein Team arbeiteten daran, nicht nur die Größe der Partikel zu kontrollieren, sondern auch, wie sie sich zusammenfügen. Sie verwendeten Kobaltoxid-Nanopartikel, eine Edelmetallalternative, die gut oxidieren kann, aber schließlich zusammendrückt und inaktiv wird.
Die Forscher applizierten Sulfationen beim Entstehungsprozess der Kobaltoxidpartikel. Die Sulfationen greifen die Partikel und bilden eine chemisch gebundene Brücke. Diese Brücke, die als Ligand bezeichnet wird, hält die Nanopartikel zusammen und hemmt gleichzeitig das Klumpenwachstum, das zu einem Verlust der katalytischen Aktivität führen würde.
Das resultierende Teilchen sah aus wie eine Himbeere: kleine Zellen, die zu etwas mehr als der Summe ihrer Teile zusammengebunden waren.
"Das Phänomen der Vernetzung zweier Substanzen wurde im Bereich der metallorganischen Rahmenforschung formuliert, aber soweit wir das beurteilen können, ist dies der erste Bericht über Oxid-Nanopartikel. Die Auswirkungen von Brückenliganden auf die Bildung von Oxid-Nanopartikeln, die hilfreich sein werden, um eine Synthesetheorie für komplexe 3D-Nanostrukturen zu etablieren", sagte Dr. Fuchigami über die himbeerförmige Nanostruktur.
Die einzigartige Oberflächen-Nanostruktur der himbeerförmigen Partikel blieb auch unter dem harten katalytischen Reaktionsprozess stabil und verbessert die Niedertemperatur-CO-Oxidationsaktivität.
Dr. Fuchigami und sein Team werden die Brückenliganden weiter untersuchen, mit dem Ziel, den Designaspekt von Nanomaterialien, wie Größe und Morphologie, präzise zu kontrollieren.
Letztendlich wollen sie die stabilste und aktivste Konfiguration für die chemische Katalyse und andere Anwendungen entdecken.
Originalveröffentlichung
Weitere News aus dem Ressort Wissenschaft
Meistgelesene News
Weitere News von unseren anderen Portalen
Verwandte Inhalte finden Sie in den Themenwelten
Themenwelt Synthese
Die chemische Synthese steht im Zentrum der modernen Chemie und ermöglicht die gezielte Herstellung von Molekülen mit spezifischen Eigenschaften. Durch das Zusammenführen von Ausgangsstoffen in definierten Reaktionsbedingungen können Chemiker eine breite Palette von Verbindungen erstellen, von einfachen Molekülen bis hin zu komplexen Wirkstoffen.

Themenwelt Synthese
Die chemische Synthese steht im Zentrum der modernen Chemie und ermöglicht die gezielte Herstellung von Molekülen mit spezifischen Eigenschaften. Durch das Zusammenführen von Ausgangsstoffen in definierten Reaktionsbedingungen können Chemiker eine breite Palette von Verbindungen erstellen, von einfachen Molekülen bis hin zu komplexen Wirkstoffen.