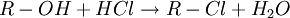Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
AminzahlUnter Aminzahl versteht man die Menge KOH in mg, die dem Aminanteil von 1g Substanz gleichgesetzt ist.
Produkt-Highlight
AllgemeinesDas Amin ist eine Verbindung die von Ammoniak ausgeht. Ein Wasserstoffatom wird durch einen organischen Alkylrest ausgetauscht. Nach der DIN 53176 wird die Aminzahl durch eine potentiometrische Titration bestimmt. Das bedeutet, dass der pH-Wert bestimmt wird.
Wässrige AminzahlAmine reagieren wie Ammoniak in wässriger Lösung.
Es wird ein Blind- und ein Hauptversuch titriert. Die Einwaage an Substanz richtet sich nach der zu erwartenden Aminzahl:
Der Verbrauch des Blindversuches wird von dem Verbrauch des Hauptversuches subtrahiert und mit der molaren Masse von KOH (56,1 g/mol) sowie der Konzentration von KOH multipliziert. Anschließend dividiert man durch die eingewogene Menge des zu bestimmenden Stoffes. Nichtwässrige AminzahlBei der nichtwässrigen Aminzahl ist das Reaktionsmedium Essigsäure Quellen
|
|||||||||||||
| Dieser Artikel basiert auf dem Artikel Aminzahl aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. |





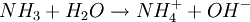 Ammoniak
Ammoniak
 Amin
Amin