Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Fluoreszenz-Korrelations-SpektroskopieDie Fluoreszenz-Korrelations-Spektroskopie (fluorescence correlation spectroscopy, FCS) ist eine höchstempfindliche optische Messmethode, die aus Fluktuationen in der Fluoreszenzintensität Informationen gewinnt. Mit FCS werden in der Regel Diffusionskonstanten, Konzentrationen und Bindungen zwischen verschiedenen diffundierenden Spezies gemessen. Die Methode wurde in den 1970er Jahren von W. W. Webb und R. Rigler voneinander unabhängig entwickelt. Produkt-Highlight
AufbauDie Grundlage für FCS bildet ein konfokales Mikroskop (siehe Abbildung). Das Anregungslicht wird mit Hilfe eines Objektives in die Probe fokussiert, sodass ein möglichst kleines Anregungsvolumen entsteht. Diffundieren nun fluoreszenzaktive Teilchen (z.B. fluoreszenzmarkierte Proteine) in das Anregungsvolumen, so werden diese dort zur Fluoreszenz angeregt. Dabei absorbieren die fluoreszenzaktiven Teilchen die Photonen des Anregungslichtes und emittieren ihrerseits Photonen größerer Wellenlänge, also geringerer Energie. Die emittierten Photonen größerer Wellenlänge können jetzt den (für das Anregungslicht undurchlässigen) Strahlteiler passieren und werden dann mit einem Fotodetektor detektiert. Wichtig für die FCS ist hierbei, dass die Detektoren mehrere Millionen mal in jeder Sekunde der Messung aufzeichnen, ob und falls ja wann genau ein Photon detektiert wurde. (Auto-) KorrelationsfunktionDie eigentliche Messgröße bei der FCS ist die Fluoreszenzintensität als Funktion der Zeit F(t), meist Trace (engl. für Spur) genannt. Die Abbildung (oben) zeigt einen Trace einer stark verdünnten Probe. Jede Spitze im Trace steht für ein fluoreszierendes Teilchen, das gerade durch das Anregungsvolumen diffundiert. Jedes dieser Teilchen braucht eine bestimmte Zeit, um den Fokus zu durchqueren. Deshalb ist die Wahrscheinlichkeit groß, dass zu aufeinanderfolgenden Abtastzeiten von ein und dem selben Teilchen Photonen detektiert werden. Man spricht davon, dass die gemessenen Intensitäten zeitlich korreliert sind. Um die Traces auszuwerten, werden sie mit sich selbst korreliert (autokorreliert). Die Autokorrelationsfunktion G(τ) ist wie folgt definiert :
Hierbei bedeuten die spitzen Klammern eine Mittelung über die Zeit, und Die Abbildung (unten) zeigt die Autokorrelation des Traces darüber, wobei man die logarithmische Skala der x-Achse beachten muss. Der Abfall der Autokorrelationsfunktion auf ihren halben Startwert ist ein Maß für die Diffusionszeit τD. Diese gibt an, wie lange ein Teilchen im Durchschnitt braucht, um das Anregungsvolumen zu durchqueren. Für die freie dreidimensionale Diffusion lässt sich zeigen, dass die Autokorrelationsfunktion wie folgt ausgedrückt werden kann: Hierbei sind Aus Für zweidimensionale Diffusion (z.B. in Zellmembranen) entfällt der Wurzelterm. Anwendungen
Literatur
|
|
| Dieser Artikel basiert auf dem Artikel Fluoreszenz-Korrelations-Spektroskopie aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. |





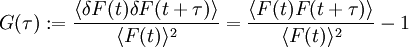 .
.
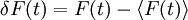 .
.
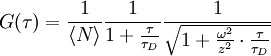
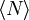 die mittlere Teilchenzahl im Anregungsvolumen (Fokus),
die mittlere Teilchenzahl im Anregungsvolumen (Fokus), 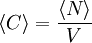 . Die Diffusionskonstante ergibt sich aus
. Die Diffusionskonstante ergibt sich aus 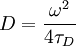 .
.


