Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Molare Leitfähigkeit
Die molare Leitfähigkeit Λm beschreibt die elektrische Leitfähigkeit einer elektrolytischen Flüssigkeit in Abhängigkeit von der Konzentration der Ionen. Sie ist definiert als Quotient Produkt-Highlightder spezifischen Leitfähigkeit Die molare Leitfähigkeit hängt von der Konzentration ab und nicht unbedingt von der Teilchenanzahl des Stoffes in Lösung. Dies liegt daran, dass die Zahl der Ionen in Lösung nicht proportional zur Konzentration des Elektrolyts sein kann. Dies ist zum Beispiel bei schwachen Elektrolyten der Fall, also bei Stoffen die in Lösung nicht vollständig dissoziieren. Ein weiterer Grund für die Abhängigkeit der Leitfähigkeit von der Konzentration ist die elektrostatische Wechselwirkung der Ionen in Lösung. Auf Grund der Wechselwirkung muss die Leitfähigkeit einer Lösung nicht proportional zur Zahl der vorhandenen Ionen sein. Typische Werte für die molare Leitfähigkeit liegen bei 10 mS·m2·mol-1. Die spezifische Leitfähigkeit ist dann über die Zellkonstante k und der gemessen Leitfähigkeit Die Zellkonstante hängt von der bei der Messung verwendeten Elektrode ab. Friedrich Wilhelm Kohlrausch fand für starke Elektrolyten bei niedriger Ionenkonzentration c das asymptotische Verhalten mit materialabhängigen Konstanten Für schwache Elektrolyte gilt das Ostwaldsches Verdünnungsgesetz. Siehe auch
Kategorien: Elektrochemie | Chemische Größe |
||||||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Molare_Leitfähigkeit aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. | ||||||||||||||||||||||||||||


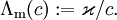



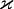 und der Ionenkonzentration c.
und der Ionenkonzentration c.
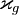 definiert:
definiert:
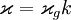
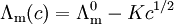
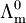 und
und 

