Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Relative FlüchtigkeitDie relative Flüchtigkeit beschreibt das Verhältnis der Flüchtigkeit der Komponenten in einem binären Gemisch. Produkt-HighlightGleichungFür Zweistoffgemische ist die relative Flüchtigkeit α wie folgt definiert:
α: Relative Flüchtigkeit Der K-Faktor ist definiert als BedeutungDie relative Flüchtigkeit ist eine wichtige Größe bei der Stofftrennung. Große relative Flüchtigkeiten erlauben eine leichte Trennung von Stoffen durch Destillation oder Rektifikation, während eine relative Flüchtigkeit von α=1 ein Azeotrop beschreibt, dass durch die beiden Verfahren nicht mehr aufgetrennt werden kann. BeispielDas binäre Gemisch aus Chloroform und Ethanol zeigt ein ausgeprägtes Azeotrop bei ca. 84 Molprozent Chloroform und P=101,325 kPa. Das Dampf-Flüssig-Gleichgewicht weist hier ein Minimum auf, die K-Faktoren kreuzen sich (K1=K2) und die relative Flüchtigkeit ist am azeotropen Punkt α=1. An diesem Beispiel ist deutlich zuerkennen, dass K-Faktoren und die relative Flüchtigkeit aus dem Dampf-Flüssig-Gleichgewicht abgeleitete Größen sind und dazu dienen, einen bestimmten Aspekt zu verdeutlichen, nämlich den Unterschied der Flüchtigkeiten der Bestandteile eines Gemischs. |
| Dieser Artikel basiert auf dem Artikel Relative_Flüchtigkeit aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. |





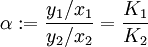
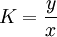 , das Verhältnis des Molenbruchs in Dampf und Flüssigkeit für eine Komponente.
, das Verhältnis des Molenbruchs in Dampf und Flüssigkeit für eine Komponente.


