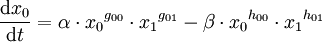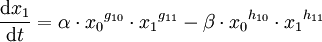Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
S-SystemS-Systeme (S für Sättigung (von Saturation) oder Synergismus) dienen zur Beschreibung und Simulation biologischer und biochemischer Systeme die einem Grenz- oder Sättigungszustand zustreben. Produkt-HighlightSie können fast alle kinetischen Phänomene natürlicher Reaktionen zuverlässig beschreiben. Die Wechselwirkungen werden durch einen Satz nichtlinearer Differentialgleichungen erster Ordnung beschrieben, die aus einem Produktions- und einem Abbauterm bestehen :
N bezeichnet die Anzahl der wechselwirkenden Substanzen. Mit xi sind die Konzentrationsvariablen bezeichnet, mit α die Produktionsrate und mit β die Abbaurate. Die Exponenten gij und hij entsprechen Reaktionsordnungen der Produktions- und Abbaufunktionen der Substanz i als Funktion der Substanz j. BeispielFür ein System mit 2 Substanzen ergibt sich folgendes Differentialgleichungssystem:
Siehe auch
Kategorien: Computerchemie | Thermodynamik | Biochemie |
| Dieser Artikel basiert auf dem Artikel S-System aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. |





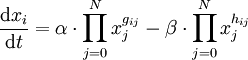 ; für i = 1 .. N
; für i = 1 .. N