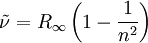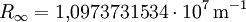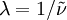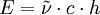Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Lyman-SerieAls Lyman-Serie wird die Folge von Spektrallinien im Spektrum des Wasserstoffatoms bezeichnet, deren Wellenzahl durch die Formel Weiteres empfehlenswertes Fachwissengegeben ist, wobei darin die Rydberg-Konstante ist, und n ganze Zahlen größer 1 sind. Die Linien der Lyman-Serie liegen im Ultravioletten und sind vor allem für Astronomen bei der Untersuchung von Sternen und Galaxien interessant. Auf der Erde können sie wegen der Absorption der Erdatmosphäre im UV Bereich nicht beobachtet werden. Sie wurden im Jahr 1906 von dem amerikanischen Physiker Theodore Lyman entdeckt. Weitere Serien sind:
Die Wellenzahl lässt sich durch die Beziehung in die Wellenlänge, bzw. durch in die entsprechende Energie umrechnen. In letzterer Formel sind c die Lichtgeschwindigkeit im Vakuum und h die plancksche Konstante. WerteFür die entsprechenden n ergibt sich eine Wellenlänge der Linien von
für n -> unendlich: 91.15 nm Die Lyman α Linie ist für Astronomen bei der Untersuchung weit entfernter Galaxien und Quasare interessant, da sich aus ihr einfach sowohl die Rotverschiebung der Objekte (bei sehr weit entfernten Objekte wird die Linie bis in den sichtbaren Bereich hinein verschoben) als auch die weiträumige Verteilung von Wasserstoff im Universum ableiten lässt. Kategorien: Atomphysik | Wasserstoffchemie |
| Dieser Artikel basiert auf dem Artikel Lyman-Serie aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. |