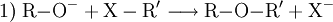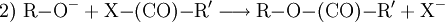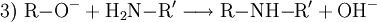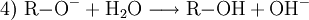Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
AlkoholateAlkoholate sind Salze aus Metall-Kationen und Alkoholat-Anionen. Die allgemeine Formel ist (RO)nMe (Me = Metall-Ion; n entspricht der Wertigkeit von diesem Ion). Alkoholat-Ionen entstehen formal durch Deprotonierung aus Alkoholen. In wässrigem Milieu können keine Alkoholate entstehen, da das Hydroxid-Ion zu schwach basisch ist, um die Hydroxyl-Gruppe der Alkohole zu deprotonieren. Deshalb werden stärkere Basen, z. B. Natriumamid oder elementares Natrium, verwendet. Verwendung finden sie unter anderem als Kondensations- und Alkylierungsmittel. Produkt-HighlightDarstellungSie entstehen z. B., wenn Alkalimetalle unter Wasserstoffentwicklung auf Alkohole einwirken:
EigenschaftenDie Alkoholate sind in Alkohol löslich, in Ether unlöslich. In reinem Zustand sind sie fest, ziehen jedoch aus der Luft Wasserdampf an und zerfließen allmählich, wobei Alkohol und Metallhydroxid entstehen, z. B. nach:
Beispiel: Natriumethanolat (Natriumäthylat) C2H5ONa, weißes bis gelbliches, hygroskopisches Pulver, entsteht durch Einwirkung von Natrium auf Ethanol (Ethylalkohol). VerwendungTechnisch finden Alkoholate Anwendung in der asymmetrischen Ether-Synthese (Williamsen-Ether-Synthese mit Halogenalkanen) (1) oder als starke Base. Mit Carbonsäurehalogeniden lassen sich Ester synthetisieren (2), mit primären Aminen erhält man sekundäre Amine (3). Bei Kontakt mit Wasser reagieren Alkoholate in einer Säure-Base-Reaktion zum entsprechenden Alkohol und Hydroxidionen. (4) Alkoholate werden hauptsächlich von der Agrar- und der Pharmaindustrie verwendet. Auch bei der Produktion von Biodiesel und Kosmetika werden Alkoholate verwenden. Kategorien: Stoffgruppe | Alkoholat |
| Dieser Artikel basiert auf dem Artikel Alkoholate aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. |





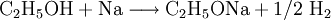
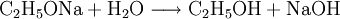 .
.