Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Carnot-WirkungsgradDer Carnot-Wirkungsgrad, auch Carnot-Faktor genannt, ist der höchste, theoretisch mögliche Wirkungsgrad bei der Umwandlung von Wärmeenergie in mechanische oder elektrische Energie. Angelehnt ist er an den vom französischen Physiker Nicolas Léonard Sadi Carnot erdachten, und nach ihm benannten, Carnot-Prozess, ein idealer Kreisprozess, der genau diesen Wirkungsgrad hat. Theoretische GrundlageProdukt-HighlightDer Wirkungsgrad einer Wärmekraftmaschine wird durch den Zweiten Hauptsatz der Thermodynamik begrenzt. Dort, wo der Prozess die Wärme auf hohem Temperaturniveau entnimmt, tritt zwangsweise eine Abnahme der Entropie ein, bei der Abgabe auf niedrigem Temperaturniveau steigt sie. Da die Entropie bei freiwillig ablaufenden Prozessen nicht abnimmt, ist damit der Anteil der Wärmeenergie vorgegeben, der nicht in Arbeit umgewandelt werden kann, sondern als Wärme auf niedrigerem Temperaturniveau abgegeben werden muss. BerechnungDer Wirkungsgrad η berechnet sich aus dem Verhältnis der höchsten (
Der Carnot-Wirkungsgrad ist umso höher, je größer das Temperaturgefälle zwischen Tatsächlich wird dieser Wirkungsgrad in der Praxis jedoch nie erreicht und liegt, je nach Kreisprozess, bei einem Drittel bis etwa zwei Drittel des Carnot-Wirkungsgrades. BeispielDer Carnot-Wirkungsgrad eines Prozesses, der zwischen 800°C und 100°C abläuft, beträgt:
|
| Dieser Artikel basiert auf dem Artikel Carnot-Wirkungsgrad aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. |





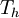 ) und der niedrigsten (
) und der niedrigsten (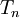 ) Temperatur des Prozesses nach der Formel:
) Temperatur des Prozesses nach der Formel:
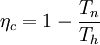 mit
mit 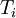 = absolute Temperaturen in
= absolute Temperaturen in