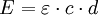Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
ExtinktionskoeffizientIn der Chemie ist der Extinktionskoeffizient (ε, Epsilon), genauer gesagt der molare, dekadische Extinktionskoeffizient (Synonym: molarer Absorptionskoeffizient) ein Maß dafür, wieviel elektromagnetische Strahlung eine spezielle Substanz in molarer Konzentration bei einer Durchtrittslänge von 1 cm und bei einer bestimmten Wellenlänge absorbiert. Dieser Begriff wird häufig in der UV/VIS-Spektroskopie bzw. Photometrie verwendet. Seinen Wert erhält man über die Gleichung
Produkt-Highlightabgeleitet von einer fundamentalen Gleichung der Photometrie, dem Lambert-Beerschen Gesetz: E bezeichnet die Extinktion, d. h. die Verminderung der Intensität, des im Photometer gemessenen Lichtes (um genau zu sein ist die Extinktion definiert als der Logarithmus des Verhältnisses der Ausgangsintensität I0 und der hinter der Probe gemessenen Intensität I, was auch als Probedurchlässigkeit bezeichnet werden kann).
Die gängige Einheit des Extinktionskoeffizienten ist L·mol-1·cm-1. Er ist abhängig von der Wellenlänge und der Temperatur bei der gemessen wird. Siehe auch
|
| Dieser Artikel basiert auf dem Artikel Extinktionskoeffizient aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. |


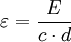 ,
,