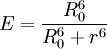Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Förster-RadiusDer Förster-Radius (nach Theodor Förster) bezeichnet den Abstand zwischen zwei Fluoreszenzfarbstoffen, bei dem zwischen diesen beiden Farbstoffen zu 50% eine strahlungsfreie Energieübertragung via FRET (Fluorescence resonance energy transfer oder auch Förster resonance energy transfer) beobachtet werden kann. Die FRET-Effizienz kann wie folgt berechnet werden: Produkt-HighlightDabei ist R0 der Förster-Radius und r der Abstand der beiden Fluoreszenzfarbstoffe. Im Falle des Fluorophorenpaars Zyan fluoreszierendes Protein (CFP) - Gelb fluoreszierendes Protein (YFP) beträgt der Förster-Radius 4,9 nm. Kategorien: Farbstoff | Spektroskopie |
| Dieser Artikel basiert auf dem Artikel Förster-Radius aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. |