Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Franck-Hertz-VersuchMit Hilfe des Franck-Hertz-Versuches von James Franck und Gustav Ludwig Hertz konnte 1914 zum ersten Mal durch ein quantenphysikalisches Experiment nachgewiesen werden, dass die Energieaufnahme oder -abgabe in Atomen nur in Form diskreter Energiepakete (Quanten) erfolgen kann. Damit konnte dieser Aspekt des Bohrschen Atommodells bestätigt werden. Für diesen Versuch wurde ihnen 1925 der Nobelpreis verliehen. Der Franck-Hertz-Versuch gehört zu den eindrucksvollsten Versuchen der Quantenlehre und ist gleichzeitig relativ einfach aufgebaut. Es ist deshalb ein sehr beliebter Demonstrationsversuch der Schulphysik. Produkt-Highlight
BeschreibungDie Quantentheorie lehrt, dass in den Atomen diskrete Energieniveaus vorhanden sind. Die Energieaufnahme oder -abgabe der Atome erfolgt als Absorption oder Emission von Energiequanten, deren Größe durch die Differenzen je zweier solcher Energieniveaus gegeben ist oder durch unelastischen Stoß mit Teilchen. Durch die Bohrsche Frequenzbedingung ist ein Zusammenhang zwischen der Anregungsenergie ΔE eines Atoms und der Emission einer Spektrallinie der Wellenlänge λ gegeben: wobei
Dies kann experimentell geprüft werden. Zur Bestimmung der niedrigsten Anregungsenergien von Atomen wird die Methode des Elektronenstoßes nach J. Franck und G. Hertz benutzt. VersuchsanordnungIn einem Glaskolben befindet sich ein Gas (z. B. Quecksilberdampf oder Neon) mit niedrigem Druck, typischerweise im Bereich von 10 bis 20 mbar. Auf einer Seite des Glaskolbens befindet sich ein Draht (Kathode K), der mittels der Spannung Uh geheizt wird. Durch die regelbare Spannung Ub erhält diese Kathode ein negatives Potential gegenüber dem Gitter G, das sich in der Mitte des Glaskolbens befindet. Auf der gegenüberliegenden Seite befindet sich eine Platte (Anode A), die gegenüber dem Gitter ein leicht negatives Potential besitzt. Die von der Kathode emittierten Elektronen werden durch das elektrische Feld zwischen Kathode und Gitter beschleunigt und nach Passieren des Gitters vom elektrischen Feld zwischen Gitter und Anode abgebremst. Der Strom zwischen Gitter und Anode wird mit Hilfe eines empfindlichen Amperemeters gemessen. AuswertungErhöht man die Spannung Ub, wachsen die gemessenen Stromwerte zunächst exponentiell, bis zu einer bestimmten Spannung. Ab dieser Spannung fällt der Strom ab, sinkt langsamer und steigt dann wieder an. Bei dem doppelten Wert der Spannung, bei der der Strom zum ersten Mal abfiel, fällt er auch dieses Mal wieder ab um dann langsamer zu sinken und schließlich wieder zu steigen. Dies wiederholt sich periodisch, dabei steigt der Strom jedes Mal höher. Dies hängt damit zusammen, dass Elektronen, sobald sie eine bestimmte Energie (bei Quecksilber ca. 4,9 eV) besitzen, beim Stoß mit den Atomen des Füllgases kinetische Energie, bei Quecksilber eben diese 4,9 eV, abgeben können. Das getroffene Atom wird dabei angeregt (Energetische Anregung), d.h. ein Hüllenelektron nimmt die abgegebene Energie auf und springt gemäß dem Bohrschen Atommodell auf eine höhere Schale. Da dieser Zustand instabil ist, fällt es unter Emission eines Lichtquants kurze Zeit später zurück in den Grundzustand. Damit lässt sich die Messung erklären: Zunächst steigt der Strom, weil das beschleunigende Feld stärker wird und mehr emittierte Elektronen die Gegenspannung überwinden, die zwischen Gitter und der Auffangplatte besteht. Dabei erfolgen elastische Stöße zwischen den Elektronen und den Gasteilchen. Wenn die Spannung die Elektronen jedoch zu stark beschleunigt, führen die beschleunigten Elektronen unelastische Stöße mit den Atomen aus und geben dabei Energie ab. Daher haben weniger von ihnen eine ausreichende kinetische Energie, um das abbremsende Feld zu überwinden. Der gemessene Strom nimmt somit ab. Er sinkt jedoch nicht wieder bis auf 0 Ampere, weil niemals alle Elektronen mit den Atomen zusammenstoßen. Beim Erhöhen der Beschleunigungsspannung werden auch die Elektronen, die beim Stoß Energie abgeben, wieder stark genug weiterbeschleunigt, sodass die Zahl der Elektronen, die die abbremsende Spannung überwinden, wieder größer wird, bis die beschleunigende Spannung die Elektronen so stark beschleunigt, dass sie ein zweites Mal die erforderlichen 4,9 eV an ein Gasteilchen abgeben können. Das besondere an diesem Ergebnis ist, dass die Elektronen eine kinetische Mindestenergie benötigen, um die Gasatome anregen zu können. Daran kann man eine Quantelung erkennen, weil immer ein bestimmter, fester Energiebetrag übertragen wird. Das von den Quecksilberatomen emittierte Licht ist mit einer Wellenlänge von ca. 253 nm im ultravioletten Bereich und damit nicht sichtbar. Zu didaktischen Zwecken wird der Versuch auch gelegentlich mit Neon anstelle von Quecksilber durchgeführt. Hier sind die Anregungsenergien zwar höher - sie liegen zwischen 18,4 eV und 19,0 eV - die Abregung geschieht jedoch auch über den Umweg über die Energiezustände im Bereich zwischen 16,6 eV und 16,9 eV. Daher entstehen auch Photonen geringerer Energie die im sichtbaren Bereich (rot-orange) liegen. Entspricht die Spannung mindestens der doppelten Anregungsspannung, so sind in der Röhre mehrere leuchtende Ebenen zu erkennen. Mit einer umgestellten Formel lässt sich so auch das plancksche Wirkungsquantum ermitteln. Literatur
|
|
| Dieser Artikel basiert auf dem Artikel Franck-Hertz-Versuch aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. |





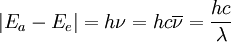
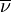 der Wellenzahl (
der Wellenzahl (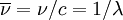 ),
),


