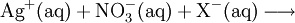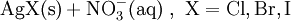Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Silbernitrat
Silbernitrat (trivial: Höllenstein, lateinisch: Lapis infernalis) ist ein Salz der Salpetersäure. Es ist zusammengesetzt aus dem Kation Ag+ und dem Nitrat-Anion NO3−. Produkt-Highlight
EigenschaftenSilbernitrat, AgNO3, bildet farblose, tafelförmige Kristalle. Es ist sehr leicht in Wasser und schwer in Ethanol löslich. Silbernitrat hat einen Schmelzpunkt von 209 °C, bei Erhitzen auf etwa 440 °C erfolgt Zersetzung unter Abscheidung von metallischem Silber und Abgabe nitroser Gase. Es muss gut verschlossen und vor Licht geschützt (beispielsweise in braunen Glasflaschen) gelagert werden, da bereits geringe Staubmengen ausreichen, um Silbernitrat unter Lichteinwirkung zu feinverteiltem Silber zu reduzieren. Sehr reines Silbernitrat ist dagegen nicht lichtempfindlich. Silbernitrat bildet mit Chlorid-, Bromid-, Iodid- und Sulfidionen schwerlösliche Niederschläge.
Silbernitrat denaturiert Eiweiß durch Bildung von Silbersalzen der Eiweiße (z. B. Silberalbuminat), in Lösungen flocken diese aus. Bei Hautkontakt bilden sich daher rasch schwarze Flecken. VerwendungSilbernitrat-Lösung ist ein Nachweisreagenz für Halogenide (Cl−-, Br−-, I−-Ionen) und Pseudohalogenide und wird zu deren quantitativen Bestimmung in der Titration nach Mohr verwendet. Fluoridionen (F−) lassen sich durch Niederschlag nicht nachweisen, da Silberfluorid als einziges Silberhalogenid gut wasserlöslich ist. Silbernitrat dient auch zum Nachweis von Aldehydgruppen und Proteinen. In der Proteinbiochemie wird Silbernitrat zum Anfärben von Proteinen verwendet, die in einem Polyacrylamid-Gel aufgetrennt wurden. In der Histologie kommt Silbernitrat zur Färbung von Gewebeschnitten, beispielsweise bei der Golgi-Cox-Methode, zum Einsatz. In der Kriminaltechnik (Daktyloskopie) wird eine Silbernitrat-Methanol-Lösung zur Sichtbarmachung von Fingerabdrücken benutzt. Ausgangsstoff zur Darstellung anderer Silbersalze, besonders der Silberhalogenide, die in der Fotografie verwendet werden. Es dient zur galvanischen Versilberung, zur Herstellung von Silberspiegeln und als Haarfärbemittel. In der Medizin kommt Silbernitrat als Antiseptikum und Adstringens (als 0,5-%ige Lösungen zur lokalen Behandlung) und als Ätzmittel („Höllenstein-Ätzstift“) gegen Hautwucherungen, Geschwüre und Warzen zur Anwendung. Bis vor einigen Jahren noch wurde Neugeborenen eine 1-%ige Silbernitratlösung in die Augen getropft um eine gonorrhoeische Augeninfektion zu verhindern (Credé-Prophylaxe). Heute wird stattdessen ein Antibiotikum gegeben, welches nicht in den Augen schmerzt und gegen mehrere unterschiedliche Keime gleichzeitig wirkt. Auf Grund der zunehmenden Antibiotika-Resistenz besteht heute die Tendenz, das Silbernitrat erneut einzusetzen. In der Homöopathie wird Silbernitrat angewendet bei extremer Angst (Gesundheit, Tod, Eile, Impulsivität, Nervosität, Prüfungsangst, Heiserkeit, Durchfall); siehe (Liste homöopathischer Grundsubstanzen). HerstellungDie Herstellung erfolgt durch Reaktion von Silber mit Salpetersäure unter Bildung nitroser Gase oder durch die Reaktion von Salpetersäure mit Silberoxid ohne Bildung nitroser Gase. Quellen
Kategorien: Ätzender Stoff | Umweltgefährlicher Stoff | Nitrat | Silberverbindung |
||||||||||||||||||||||||||||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Silbernitrat aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. | ||||||||||||||||||||||||||||||||||||||||||||||||||