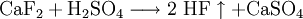Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Calciumfluorid
Calciumfluorid (auch Kalziumfluorid, eigentlich Calciumdifluorid) ist ein Calcium-Salz der Fluorwasserstoffsäure. Weiteres empfehlenswertes Fachwissen
EigenschaftenCalciumfluorid bildet farblose, in Wasser und verdünnten Säuren schwerlösliche Kristalle. Natürlich vorkommendes Calciumfluorid heißt Fluorit oder Flussspat und ist meist durch Verunreinigungen gelb, grün, blau oder violett gefärbt.
Calciumfluorid kristallisiert in dem weitverbreiteten Fluoritgitter.
In den meisten Lösungsmitteln wie Wasser, Alkohol usw. ist es unlöslich. Für Ultraviolett- und Infrarotstrahlung besitzt es eine hohe Durchlässigkeit. Reaktionen
Vorkommen und GewinnungFlussspat wird in großen Mengen, mehrere Millionen Tonnen pro Jahr, im Tage- und Tiefbau bergmännisch gewonnen. Da es mit anderen Mineralien wie Schwerspat (Bariumsulfat BaSO4, Bleiglanz PbS und Quarz SiO2) vergesellschaftet ist, muss das 30–60 % CaF2 enthaltende Roherz vor einer industriellen Verwertung aufgearbeitet werden. Hierzu wird das geförderte Erz mechanisch zerkleinert und anschließend durch (mehrstufige) Flotation auf bis zu 98 % aufkonzentriert. Als Handelsform unterscheidet man
Reines Calciumfluorid gewinnt man durch Umsatz von Fluorwasserstoff oder Hexafluorokieselsäure mit Calciumsalzen. VerwendungCalciumfluorid ist neben den Fluoriden aus der Phosphorsäureherstellung der wichtigste Rohstoff zur Fluorherstellung. Entsprechend den oben genannten Flussspatqualitäten wird Calciumfluorid für folgende Anwendungen verwendet:
Weitere Anwendungen:
VorsichtsmaßnahmenBei Kontakt mit starken Säuren wird Fluorwasserstoff freigesetzt. Verätzungsgefahr. NachweisÄtzprobe: CaF2 mit etwas 6n Schwefelsäure in ein Reagenzglas geben. Die Benetzung der Glasoberfläche ändert sich, da Fluorwasserstoffsäure HF entsteht. QuellenKategorien: Calciumverbindung | Fluorid |
|||||||||||||||||||||||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Calciumfluorid aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. | |||||||||||||||||||||||||||||||||||||||||||||