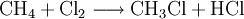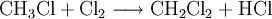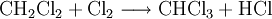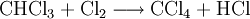Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Chlormethan
Methylchlorid oder Chlormethan ist ein farbloses, schwach süßlich riechendes, gesundheitsschädliches und leicht brennbares Gas. Weiteres empfehlenswertes Fachwissen
GewinnungChlormethan kann durch Erhitzen von Chlor mit Methan auf 400–500 °C erzeugt werden. Bei dieser Temperatur findet eine schrittweise radikalische Substitution bis hin zu Tetrachlormethan statt:
Das Ergebnis des Prozesses ist eine Mischung der vier Chlormethane, welche durch Destillation getrennt werden können. Technisch wird Methanol hydrochloriert. VerwendungEs wird als Methylierungsmittel in der organischen Chemie eingesetzt und zur Veretherung von Alkoholen und Phenolen. Es wird in der Silikonherstellung benötigt. Seine hohe Verdampfungswärme ermöglicht einen Einsatz als Kältemittel. Früher wurde es zu Narkosezwecken, aber auch als lokales Kälteanästhetikum, verwendet. GefahrenDas betäubende Gas löst Störungen des Zentralnervensystems aus und schädigt Leber, Niere und Herz. Methylchlorid gilt als Stoff mit begründetem Verdacht auf krebserzeugendes Potenzial und der Fruchtschädigung. Die Explosionsgrenze liegt zwischen 7,1 Vol.-% und 18,5 Vol.-% in der Luft. Quellen
Kategorien: Gesundheitsschädlicher Stoff | Feuergefährlicher Stoff | Organochlorverbindung | Halogenalkan | Gas |
||||||||||||||||||||||||||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Chlormethan aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. | ||||||||||||||||||||||||||||||||||||||||||||||||