Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
ElektronenspinresonanzMithilfe der Elektronenspinresonanz (kurz: ESR oder EPR für Electron Paramagnetic Resonance) wird die resonante Mikrowellenabsorption einer Probe in einem äußeren Magnetfeld gemessen. Dies macht sie zu einer hervorragend geeigneten Methode zur Untersuchung von Proben, die über ein permanentes magnetisches Moment (ungepaarte Elektronen) verfügen. Weiteres empfehlenswertes FachwissenDas erste ESR-Experiment wurde von Jewgeni Konstantinowitsch Sawoiski in Kasan 1944 durchgeführt. Bei paramagnetischen Salzen wie Kupfersulfat und Manganchlorid beobachtete er Resonanzabsorption der eingestrahlten Energie bei definierten Verhältnissen der Stärke des statischen Magnetfeldes zur Frequenz. Um dieses allererste ESR-Spektrometer bauen zu können, hatte Sawoiski das Klystron aus dem Radargerät eines erbeuteten deutschen Panzers benutzt. Bringt man eine Probe mit permanentem magnetischem Moment in ein Magnetfeld, so spalten sich die entarteten Energiezustände auf (Zeeman-Effekt). Oft wird der Zeemaneffekt anhand von Übergängen zwischen Niveaus unterschiedlicher Hauptquantenzahl untersucht; bei der ESR werden dagegen Übergänge zwischen Niveaus gleicher Hauptquantenzahl beobachtet: Durch Bestrahlung mit einer Mikrowelle, deren Energie der Aufspaltung der Niveaus entspricht, kommt es zur Absorption. In der Praxis wird die zu untersuchende Probe in einem veränderlichen Magnetfeld mit einer Mikrowelle fester Frequenz bestrahlt. Das aufgezeichnete Absorptionsspektrum erlaubt Rückschlüsse auf die magnetische Umgebung der magnetische Momente (siehe g-Faktor). In der ESR-Spektroskopie können nur Substanzen mit einem oder mehreren ungepaarten Elektronen untersucht werden. Typische Beispiele hierfür sind:
Resonanz-AbsorptionEin statisches (meist homogenes) Magnetfeld, in dem sich Atome oder Moleküle mit nicht abgeschlossenen elektronischen Schalen befinden, hebt die magnetische Entartung der Zustände auf (Zeeman-Effekt). Diese Aufspaltung ist in erster Näherung proportional zum angelegten Magnetfeld H: mJ ist dabei die magnetische Quantenzahl. Jedes magnetische Energieniveau besitzt deshalb den Abstand E0 = gμ0μBH vom nächsten benachbarten Zustand (äquidistante Aufspaltung). Zwischen den Zuständen sind magnetische Dipolar-Übergänge zwischen benachbarten Niveaus möglich ( Bei der paramagnetischen Resonanz ergibt sich daraus die Resonanzbedingung Der so genannte G-Faktor (oder Landé-Faktor) verknüpft die Größe des magnetischen Moments eines Atoms mit seinem Gesamtdrehimpuls. Für reinen Bahnmagnetismus (s = 0) ist g = 1, für reinen Spinmagnetismus (l = 0) gilt g = 2 (genauer 2,002322). Allgemein lässt sich folgende Beziehung angeben:
Diese Formel kann aus dem Vektormodell der Atomphysik hergeleitet werden. Siehe auch
|
| Dieser Artikel basiert auf dem Artikel Elektronenspinresonanz aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. |





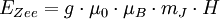
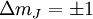 ). Legt man senkrecht zum statischen Magnetfeld ein hochfrequentes Wechselfeld (z.B. bei
). Legt man senkrecht zum statischen Magnetfeld ein hochfrequentes Wechselfeld (z.B. bei 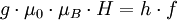
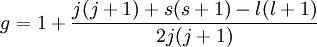 .
.


