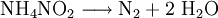Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Ammoniumnitrit
Ammoniumnitrit ist ein Salz der Salpetrigen Säure. Obwohl er die Form von nadelförmigen, farblosen Kristallen annimmt, ist der Stoff sehr instabil. Er oxidiert bereits bei Raumtemperatur sehr leicht am Luftsauerstoff, durch eine hohe Feuchtigkeit kann dies nochmals stark beschleunigt werden – die Kristalle verfärben sich gelblich. Produkt-HighlightGefahrenErhitzt man das Ammoniumnitrit in seiner Kristallform, explodiert es ab einer Temperatur von 60–70 °C. Es reichen jedoch bereits auch kleinere Stöße aus, um spontane Explosionen hervorzurufen. Aufgrund dieser Umstände ist der Transport von Ammoniumnitrit generell verboten. ReaktionenAmmoniumnitrit zerfällt zu Stickstoff und Wasser: VerwendungAmmoniumnitrit kann zur Synthese von Hydroxylamin verwendet werden. Ebenfalls eignet es sich als feste Stickstoffquelle, um beispielsweise Salze von NH3OH zu synthetisieren. Kategorien: Ammoniumverbindung | Nitrit |
||||||||||||||||||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Ammoniumnitrit aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. | ||||||||||||||||||||||||||||||||||||||||