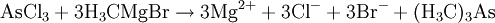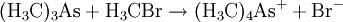Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
ArsineArsine sind organische Arsen-Verbindungen. Ersetzt man formal in den Arsanen (Arsenwasserstoffen) die Wasserstoff-Atome durch organische Reste, so erhält man Arsine ("organische Arsane"). Produkt-HighlightVielfach werden diese Verbindungen etwas unpräzise als Arsane bezeichnet, um sie als Derivate der Arsenwasserstoffe zu kennzeichnen. Monoarsan wird häufig nach alter Nomenklatur Arsin genannt. GeschichteCadet de Gassicourt erhitzte 1760 Arsenik im Beisein von Kaliumacetat. Dabei entstand ein Gemisch aus Kakodyl (Tetramethyldiarsan) und Kakodyloxid (Oxybis-dimethylarsan). Gewinnung und DarstellungTertiäre Arsine (ausgehend vom Monoarsan werden alle drei Wasserstoff-Atome gegen organische Reste ausgetauscht: AsH3 → AsR3) können aus Arsen(III)-chlorid mit Hilfe metallorganischer Reagenzien wie Grignard-Verbindungen gewonnen werden:
EigenschaftenArsine sind nicht beständig gegenüber Luftsauerstoff. Zum Teil entzünden sie sich spontan. Sie reagieren leicht mit Alkylhalogeniden unter Anlagerung von einem weiteren Alkylrest zu einem quartären, das heißt vier organische Reste tragenden Arsoniumsalz:
Arsine sind schwache Lewis-Basen. Mit Übergangsmetallen können sie eine Vielzahl von Komplexen bilden, mit Sauerstoff, Schwefel und Halogenen Verbindungen des Typs R3AsO, R3AsS und R3AsCl2. |
| Dieser Artikel basiert auf dem Artikel Arsine aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. |