Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
EmulsionspolymerisationBei der Emulsionspolymerisation wird die Polymerisationsreaktion wenig wasserlöslicher Monomere (z. B. von Styrol zu Polystyrol) in einer wässrigen Emulsion des Monomers durchgeführt. Es werden Polymerpartikel erhalten, die um Größenordnungen kleiner sind als die Monomertröpfchen bei Reaktionsbeginn. Um dies zu erreichen, werden verschiedene Hilfsstoffe eingesetzt. Produkt-Highlight
AllgemeinesWichtig zur Lösungsvermittlung des hydrophoben Monomers ist der Emulgator. Mit Hilfe solcher amphiphiler Verbindungen wird die Stabilisierung des Monomers in Wasser erst ermöglicht. Ein gebräuchlicher Emulgator ist z. B. SDS (engl. sodium dodecylsulfate = Natriumdodecylsulfat). Des Weiteren wird bei der radikalischen Emulsionspolymerisation ein wasserlöslicher Initiator eingesetzt. Dieses Polymerisationsverfahren hat industriell eine große Bedeutung. Beispielsweise werden PVC, Polystyrol-, Polyacrylat- und Polyvinylacetatcopolymere auf diese Art hergestellt. Ersters wird hieraus durch Ausfällung isoliert, während die anderen meist direkt eingesetzt werden, z.B. als Bindemittel für wässrige Dispersionsfarben. ReaktionsprinzipZunächst löst man den Emulgator in Wasser. Bei einer bestimmten Konzentration (KMK kritische Mizellenkonzentration) des Emulgators bilden sich Mizellen aus, in denen später die Polymerketten wachsen können. Man gibt dann noch das Monomer zu und erzeugt zum Schluss reaktive Radikale. Dies kann dadurch geschehen, dass man einen thermisch zerfallenden Radikalbildner (meist Peroxide oder Azo-Verbindungen) zugibt und die Mischung über dessen Zerfallstemperatur erwärmt. Alternativ kann man Radikale auch ohne thermische Anregung durch photochemische Zersetzung (z.B. Azobisisobutyronitril AIBN) oder geeignete Redoxreaktionen (z.B. zwischen Ammoniumperoxidisulfat und Ascorbinsäure) erzeugen. Zunächst bilden sich kleine Polymerradikale in der Wasserphase, die nach Anlagerung einiger der schwerer wasserlöslichen Monomeren eine Affinität zu dem hydrophoben Mizellinneren entwickeln und dahin diffundieren, sodass die Reaktion dann dort fortschreitet. Auch kann ein initial erzeugtes Polymerteilchen Emulgator anlagern und so um sich herum eine Micelle bilden. In den Mizellen bilden sich dann sog. Latexpartikel. Die Mizellenwand aus Emulgator wirkt im Prinzip wie eine Membran, sodass weitere Monomere in die Mizelle diffundieren können, um die Polymerisation voranzutreiben. Weitere Emulgatormoleküle treten hinzu und lassen die Mizellenwand gleichsam mitwachsen. Unter der Voraussetzung, dass Initiator im Überschuss vorhanden ist, kommt die Polymerisation erst zum Erliegen, wenn das Monomer komplett verbraucht ist. Es ist zwar theoretisch denkbar, daß auch in den Monomerentröpfchen im Reaktionsansatz eine Polymerisation stattfindet, jedoch ist deren Konzentration im Gegensatz zu den Micellen um einige Größenordnungen kleiner. So ist diese Reaktion sehr unwahrscheinlich, da es nur selten zu einem Kontakt eines Polymerradikals oder Initiatorradikals kommt. KinetikDie Kinetik solcher Verfahren ist kompliziert. Folgende Näherung gilt bei Umsätzen unter 60%: Die Bruttoreaktionsgeschwindigkeit ergibt sich zu:
Mit N: Micellenzahl kw: Geschwindigkeitskonstante der Wachstumsreaktion [M]: Monomerenkonzentration. Die Reaktionsgeschwindigkeit hängt also von der Micellenzahl und damit von der Emulgatorkonzantration ab. PolymerisationsgradGenähert kann der Polymerisationsgrad angegeben werden zu
Somit ist der Polymerisationsgrad über die Anzahl der Latexpartikel und damit über die Emulgatorkonzentration steuerbar. Vor- und NachteileDie Vorteile der Emulsionspolymerisation sind:
Dem gegenüber stehen folgenden Nachteile:
LiteraturB. Philipp, G. Reinisch: Grundlagen der makromolekularen Chemie. Vieweg 1976. E. Fitzer, W. Fritz, G. Emig: Technische Chemie. Springer 1995. Siehe auch |
|
| Dieser Artikel basiert auf dem Artikel Emulsionspolymerisation aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. |





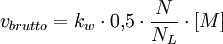 .
.
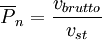 .
Mit
.
Mit 

