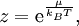Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
FugazitätDie Fugazität stellt eine begriffliche Hilfe bei der Bestimmung des chemischen Potentials realer Gase dar. Produkt-HighlightSie kann als effektiver Druck des realen Gases aufgefasst werden, welches im Zusammenhang einer Druckänderung betrachtet wird. Speziell von Vorteil ist die Verwendung der Fugazität bei der Bestimmung der Gibbs-Energie für den Zustand des realen Gases nach der Druckänderung. Eine andere anschauliche Erklärung ist, dass die Fugazität die Neigung des Moleküls, das System zu verlassen, angibt. Das erklärt auch den Begriff selbst, vom lateinischen fugere (= fliehen). Definition aus der statistischen PhysikIn der statistischen Physik, die die Grundlage der Themodynamik bildet, taucht die Fugazität z als Faktor beim Übergang von der kanonischen Zustandssumme Z(T,V,N) (die Systeme mit konstanter Teilchenzahl N beschreibt) zur großkanonischen Zustandssumme Ξ(T,V,μ) (die zur Beschreibung von Systemen mit variabler Teilchenzahl geeignet ist) auf[1]:
Die Fugazität z ist dabei gegeben als wobei kB die Boltzmann-Konstante ist. Die Fugazität kann also als Funktion der Temperatur und des chemischen Potentials angesehen werden. LiteraturPeter W. Atkins: Physikalische Chemie, 2. Auflage, Wiley-VCH, Weinheim 1996, ISBN 3-527-29275-6 Quellen und Weblinks
|
| Dieser Artikel basiert auf dem Artikel Fugazität aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. |





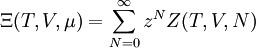 , wobei
, wobei