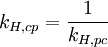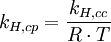Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Henry-GesetzDas Henry-Gesetz (nach dem englischen Chemiker William Henry) beschreibt das Löslichkeitsverhalten von (flüchtigen) Substanzen in einer Flüssigkeit. Produkt-HighlightEs besagt, dass die Konzentration eines Gases in einer Flüssigkeit direkt proportional zum Partialdruck des entsprechenden Gases über der Flüssigkeit ist. Die Proportionalität wird durch die Henry-Konstante ausgedrückt. Die am häufigsten verwendete Schreibweise ist: (p: Partialdruck der Substanz, cl: Konzentration in der Lösung, kH,pc: Henry-Konstante) Es ist mit dem Prinzip von Le Châtelier vereinbar, denn auf eine äußere Druckzunahme wird das System mit einer Verkleinerung der Gasteilchenanzahl reagieren (und den Druck somit wieder vermindern, bzw. dem "Zwang" ausweichen). Verschiedene Versionen
Die verschiedenen Henry-Konstanten lassen sich ineinander umrechnen, beispielsweise ergibt sich für oder wobei R die molare Gaskonstante ist und T die Temperatur des Systems. Grenzen der GültigkeitStrenggenommen ist das Henry Gesetz nur für kleine und mäßige Drücke bis ungefähr 5 Bar anwendbar. Auch ist es nur bei verdünnten Lösungen (das heißt bei niedrigen Partialdrücken) gültig. Zudem darf das gelöste Teilchen nicht mit dem Lösungsmittel reagieren, wie zum Beispiel Kohlenstoffdioxid, welches zu Kohlensäure reagiert und dem Gleichgewicht entzogen wird. Anwendung im TauchsportMit dem relativ einfachen Henry-Gesetz lässt sich die Dekompressionserkrankung bei Tauchern erklären. Der Umgebungsdruck nimmt um etwa 1 bar pro 10 Meter Wassertiefe zu. Damit löst sich der in der Atemluft enthaltene Stickstoff zunehmend besser im Blut. Taucht der Taucher jedoch zu schnell wieder auf, nimmt die Löslichkeit des Gases im Blut gemäß dem Henry-Gesetz rapide ab und der Stickstoff gast aus. Die entstehenden Gasbläschen behindern die Blutströmung und führen zur Dekompressionserkrankung. |
|||||||||||||||
| Dieser Artikel basiert auf dem Artikel Henry-Gesetz aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. |





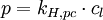
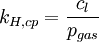
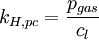
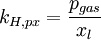
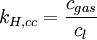
![\left[\frac{mol_{gas}}{l \cdot atm}\right]](images/math/5/0/e/50e99539c80598c06fa55e3180440807.png)
![\left[\frac{l \cdot atm}{mol_{gas}}\right]](images/math/5/8/c/58c56cd7a5cb9ebf14584b5dbbb29463.png)
![\left[\frac{atm \cdot mol_{wasser}}{mol_{gas}}\right]](images/math/6/0/b/60bfcd6e7ff26c94fb70e1f5034b91d1.png)
![\left[ dimensionslos \right]](images/math/e/6/5/e6583e6870b37f9dbd7a68b91e387437.png)