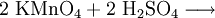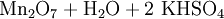Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Mangan(VII)-oxid
Mangan(VII)-oxid ist eine chemische Verbindung mit der Summenformel Mn2O7. Die ölige Flüssigkeit ist hochreaktiv, da sie (wie die meisten ladungsneutralen Oxide) ein gefährlicher Oxidator (siehe auch Oxidationsmittel) ist. Die erste Beschreibung erfolgte 1860[2]. Produkt-Highlight
Gewinnung und DarstellungMangan(VII)-oxid wird durch die Reaktion von Schwefelsäure mit Kaliumpermanganat gewonnen. EigenschaftenBei niedrigen Temperaturen liegt die Verbindung als kristalliner Feststoff vor, der grünes Licht reflektiert und bei Durchlicht rot aussieht. Die Verbindung besteht aus aus einem Paar Tetraeder die über ein Sauerstoff-Teilchen verbunden sind, was mit der Strukturformel O3Mn–O–MnO3 beschrieben werden kann. Die außenliegenden Mn–O–Verbindungen haben einen Abstand von 1,585 Å und die zentrale Brücke 1,77 Å. Die zentrale Mn–O–Mn–Brücke hat einen Winkel von 120,7°[3]. Diese Eigenschaften sind ähnlich wie die von Pyrosulfaten, Pyrophosphaten, Dichromaten und anderen R2O7–Verbindungen (wobei R für Chlor oder Metalle wie Technetium oder Rhenium[4] steht). SicherheitshinweiseMangan(VII)-oxid ist eine hochreaktive Verbindung. Sie zersetzt sich bei Raumtemperatur und explodiert ab Temperaturen von etwa 55 °C, wobei die Explosion auch durch Schlag oder Verunreinigungen ausgelöst werden kann. Es entstehen dabei Mangan(IV)-oxid (Braunstein) und Sauerstoff, sowie geringe Mengen an Ozon, was der Verbindung einen starken Geruch verleiht. Sie verkohlt organische Stoffe, wie etwa Holz, sofort. Mit Aceton oder anderen Lösungsmitteln erfolgt Selbstentzündung. Quellen
siehe auchKategorien: Explosionsgefährlicher Stoff | Ätzender Stoff | Oxid | Manganverbindung |
||||||||||||||||||||||||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Mangan(VII)-oxid aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. | ||||||||||||||||||||||||||||||||||||||||||||||