Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
OktaederlückeDie Oktaederlücke ist der Hohlraum in einem Oktaeder, der frei bleibt, wenn in die Ecken des Oktaeders sich berührende Kugeln gesetzt werden.
Produkt-HighlightViele Kristalle bestehen aus Gittern, in denen die Atome lokal einen Oktaeder bilden. Zu diesen Kristallgittern gehören das kubisch-flächenzentrierte Gitter und das kubisch-raumzentrierte Gitter. Kleinere Fremdatome können in diese Oktaederlücken eingelagert werden. Diese können dabei unregelmäßig als Fehlstellen oder regelmäßig als Verbindungspartner eingebaut werden. Ein Beispiel für den regelmäßigen Einbau ist die Natriumchlorid-Struktur. Im Natriumchlorid sind die Chlorid-Anionen etwa doppelt so groß wie die Natrium-Kationen. Die Anionen bilden ein dichtgepacktes kubisch-flächenzentriertes Gitter, die Kationen füllen dabei die Oktaederlücken auf. Die Größe der Oktaederlücke kann angegeben werden durch den Radius r der größten Kugel, die in die Lücke hineinpasst. Mit dem Umkugelradius des Oktaeders und dem Radius R der großen Kugeln in den Ecken des Oktaeders und der Seitenlänge a = 2 R des Oktaeders erhält man für die Oktaederlücken des kubisch-flächenzentrierten Gitters
Siehe auch: Tetraederlücke |
||||||
| Dieser Artikel basiert auf dem Artikel Oktaederlücke aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. | ||||||





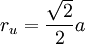
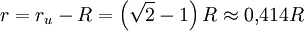 .
.


