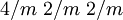Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Rutil
Rutil ist ein im tetragonalen Kristallsystem kristallisierendes Oxid-Mineral mit einer Härte von 6 bis 6,5, einer rotbraunen bis schwarzen, manchmal auch gelben, bläulichen oder violetten Farbe und einer meist gelben bis blassbraunen Strichfarbe. Es ist die bedeutendste der drei Modifikationen des Titandioxids TiO2; die beiden anderen sind Anatas und Brookit. Produkt-Highlight
Etymologie und GeschichteBenannt wurde Rutil nach dem lateinischen Wort rutilus für rot oder rötlich, als Hinweis für seine häufig vorkommende Färbung. Bis 1795, als seine chemische Zusammensetzung bekannt wurde, wurde Rutil fälschlicherweise für ein Mineral der Turmalingruppe gehalten. Er wurde von Abraham Gottlob Werner benannt. Die ersten synthetischen Rutile wurden 1948 produziert. Modifikationen und VarietätenRutil ist die einzige bei hohen Temperaturen stabile Modifikation des Titandioxid. Flache, netz- bis gitterartige Verwachsungen von nadelartigen feinen Rutilzwillingen werden als Sagenit, eisenhaltiges Rutil als Nigrin bezeichnet. Bildung und FundorteRutil kommt sowohl massiv als auch in Form prismatischer Kristalle vor. Man findet ihn auch als feine Nadeln in anderen Mineralen wie Korund oder Quarz, in letzterem Fall wird er auch Venushaar genannt. So genannte Sternensaphire oder Sternenrubine enthalten feine Rutilnadeln, an denen das Licht gebrochen wird; dieses optische Phänomen wird als Asterismus bezeichnet. Rutil ist in vielen magmatischen Gesteinen als akzessorisches Mineral enthalten, daneben kommt er in metamorphen Gesteinen und in Flusssedimenten vor. Fundorte sind unter anderem Burkina Faso und Tsumeb/Nigeria in Afrika Kitaa in Grönland, Wales in Großbritannien, sowie verschiedene Staaten in den USA und Kanada. [1] Verwendungals RohstoffRutil ist mit einem Metall-Gehalt von etwa 60 Prozent nach Ilmenit das bedeutendste Titan-Mineral. Künstlich hergestellt kann er als Schmuckstein Verwendung finden. Titandioxid in der Rutil-Modifikation wird auf Grund der hohen Lichtbrechung als Weißpigment verwendet. Rutil wird außerdem allein oder in Verbindung mit Zellulose zum Umhüllen von Elektroden für das Lichtbogenschweißen eingesetzt und dient dabei dazu, die Schweißung zu verbessern oder erst zu ermöglichen. als SchmucksteinRutil selbst wird nicht oder nur gelegentlich von Sammlern zu Schmucksteinen verarbeitet. Das Mineral sorgt jedoch als eingeschlossener Bestandteil vieler Schmuck-Minerale für verschiedene optische Effekte wie beispielsweise Asterismus (Sternförmige Lichtreflexe) und Chatoyance (Katzenaugeneffekt). Siehe auchEinzelnachweise
Literatur
Kategorien: Mineral | Oxide und Hydroxide | Tetragonales Kristallsystem | Titanmineral |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Rutil aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||