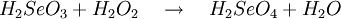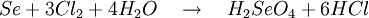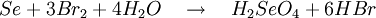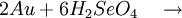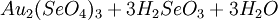Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Selensäure
Produkt-HighlightGewinnungDie Selensäure kann auf zwei verschiedene Arten dargestellt werden. Eine Möglichkeit ist die Oxidation von seleniger Säure (H2SeO3) mit Wasserstoffperoxid (H2O2), KMnO4 oder HClO3: In der Regel wird jedoch elementares Selen mit Chlor- oder Bromwasser oxidiert: EigenschaftenReine Selensäure bildet farblose Kristalle, die bei etwa 60 °C schmelzen. Selensäure hat chemisch gesehen große Ähnlichkeit mit der Schwefelsäure, wirkt jedoch stärker oxidierend. Sie ist eine starke Säure und wirkt hygroskopisch. Dies bedeutet, dass sie organische Substanzen durch Wasserentzug verkohlt und zur Trocknung von Flüssigkeiten und Gasen benutzt werden kann. Selensäure ist wie Königswasser in der Lage, Gold oder Platin zu lösen: Kategorien: Giftiger Stoff | Ätzender Stoff | Mineralsäure | Selenverbindung |
|||||||||||||||||||||||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Selensäure aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. | |||||||||||||||||||||||||||||||||||||||||||||