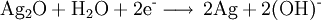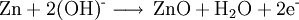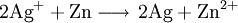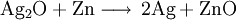Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Silberoxid-Zink-BatterieSilberoxid-Zink-Zellen sind Primärzellen, die in Form von Knopfzellen im Handel sind. Produkt-HighlightDie Anode einer Silberoxid-Zink-Zelle besteht aus Zinkpulver, das im Verlauf der Entladung oxidiert wird. Die Katode besteht aus Silberoxid, das beim Entladen zu elementarem Silber reduziert wird. Als Elektrolyt kommt verdünnte Kalilauge zum Einsatz. Die Nennspannung einer solchen Zelle beträgt etwa 1,5 V. Vereinfacht laufen bei der Entladung folgende Reaktionen ab:
Die Silberoxid-Zink-Zelle ist eine Primärzelle und lässt sich daher nicht wieder aufladen. Beim Aufladen würde sich der Elektrolyt zersetzen, was meist zur Zerstörung der Batterie führt. |
| Dieser Artikel basiert auf dem Artikel Silberoxid-Zink-Batterie aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. |