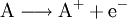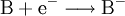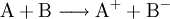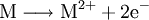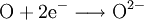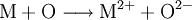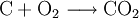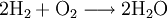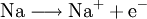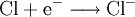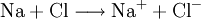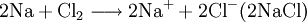Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Oxidation
Die Oxidation (oder Oxydation) ist eine chemische Reaktion, bei der ein zu oxidierender Stoff (Elektronendonator) Elektronen abgibt. Ein anderer Stoff (Oxidationsmittel) nimmt die Elektronen auf (Elektronenakzeptor). Dieser wird durch die Elektronenaufnahme reduziert. Mit der Oxidation ist also immer auch eine Reduktion verbunden. Beide Reaktionen zusammen werden als Teilreaktionen einer Redoxreaktion betrachtet.
Produkt-Highlight
GeschichteDer Begriff Oxidation wurde ursprünglich von Antoine Laurent de Lavoisier geprägt, der damit die Vereinigung von Elementen und chemischen Verbindungen mit dem Element Sauerstoff (Oxygenium franz: oxygene), also die Bildung von Oxiden beschreiben wollte. Später erfolgte eine Erweiterung des Begriffes, indem man Reaktionen, bei denen Wasserstoff-Atome einer Verbindung entzogen wurden (Dehydrierung), mit einbezog. Auf Grundlage der Ionentheorie und des Bohrschen Atommodells konnte die Oxidation schließlich unter elektronentheoretischen Gesichtspunkten interpretiert und verallgemeinert werden. Das Charakteristische an diesem Vorgang wird nun in der Elektronenabgabe eines chemischen Stoffes gesehen. Früher wurde die Oxidation als Calzination bezeichnet. Oxidation durch Sauerstoff
Ursprüngliche Bedeutung und Erweiterung des BegriffsAls Oxidation im ursprünglichen Sinn bezeichnete man früher die chemische Reaktion eines Stoffes mit Sauerstoff. Aber auch heute noch assoziiert man mit diesem Begriff vielfach die Umsetzung mit Sauerstoff und die Bildung von Oxiden. Jedoch ist im Rahmen der allgemeineren Definition diese Reaktion nur eine von vielen, die sich mit Hilfe der Valenzelektronentheorie erklären lässt. Reagiert z. B. ein Metallatom mit einem Sauerstoff-Atom, so kann man die Oxidation des Metalls und somit die Metalloxidbildung anhand folgender Reaktionsgleichungen nachvollziehen:
Sauerstoff hat in diesem Fall das Bestreben, durch Aufnahme von zwei Elektronen eine stabile Valenzelektronenschale mit insgesamt acht Elektronen aufzubauen (Oktettregel). Das Metall wiederum kann durch Abgabe der Elektronen teilbesetzte Schalen auflösen und so die nächst niedrigere stabile Elektronenkonfiguration erreichen. Beispiele der Oxidation durch Sauerstoff
Oxidation ohne SauerstoffDer Begriff der Oxidation wurde später auf Reaktionen erweitert, die nach dem gleichen chemischen Prinzip ablaufen, auch wenn kein Sauerstoff daran beteiligt ist. Im weiteren Sinne bedeutet Oxidation das Abgeben von Elektronen. Zum Beispiel gibt bei der Reaktion von Natrium und Chlor zu Natriumchlorid das Natriumatom ein Elektron an das Chloratom ab, Natrium wird also oxidiert. Im Gegenzug wird Chlor dabei reduziert.
Da Chlor nur molekular als Cl2 in die Reaktion eingeht, schreibt man genauer OxidationszahlDie Oxidationszahl wird als hypothetische Ladungszahl eines Atoms oder einer Atomgruppe (Molekül) definiert. Bei der Oxidation wird die Oxidationszahl erhöht (Na0 → Na+I), bei der Reduktion erniedrigt. Bei einem Molekül wird/werden das/die bindende(n) Elektronenpaar(e) dem Atom zugesprochen, dessen Elektronegativität höher ist. Zahlen gleichartiger Atomverbindungen werden untereinander gleich aufgeteilt. Ionen haben als Summe ihrer Oxidationszahlen ihre Ladungszahl, Moleküle die Summe 0. Bedeutend sind die Oxidationszahlen jener Atome, die Bestandteil einer funktionellen Gruppe sind. Oxidation in der BiologieVor allem in der Biologie definiert man Oxidation als „Abgabe von Wasserstoff“. Bei vielen biochemischen Vorgängen in der Zelle, z. B. der Glycolyse werden organischen Verbindungen Wasserstoffatome durch bestimmte Coenzyme (NAD, NADP, FAD) „entrissen“. siehe auch
|
|
| Dieser Artikel basiert auf dem Artikel Oxidation aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. |