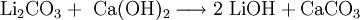Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Lithiumhydroxid
Lithiumhydroxid LiOH, das Hydroxid des Lithiums, ist zwar eine starke, in Wasser aber nur mäßig lösliche Base. Weiteres empfehlenswertes Fachwissen
SyntheseReines Lithiumoxid Li2O reagiert mit Wasser zu Lithiumhydroxid. Die technische Herstellung erfolgt durch Umsetzung von Lithiumcarbonat mit Calciumhydroxid: ReaktionsverhaltenLithiumhydroxid ist eine starke Base und reagiert als solche mit Säuren. Außerdem ist Lithiumhydroxid fähig Kohlendioxid zu binden (1 g wasserfreies Lithiumhydroxid bindet 450 ml CO2). VerwendungLithiumhydroxid wird in Akkus, in Fotoentwicklern, zur Darstellung von Boran-Raketentreibstoffen und zur Herstellung stark wasserabweisender Schmierfette auf Lithiumstearatbasis verwendet. Durch seine Eigenschaft, Kohlendioxid zu binden, wird es als Luftreiniger in U-Booten, Fliegeratemgeräten und Raumschiffen verwendet. Im Kühlmittel von Druckwasserreaktoren wird es gegenüber der Borsäure als Alkalisierungsmittel eingesetzt. Quellen
Kategorien: Ätzender Stoff | Lithiumverbindung | Hydroxid |
|||||||||||||||||||||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Lithiumhydroxid aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. | |||||||||||||||||||||||||||||||||||||||||||