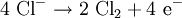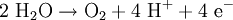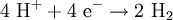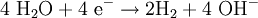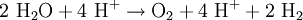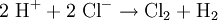Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Überspannung (Elektrochemie)
Produkt-HighlightIn der Elektrochemie ist die Überspannung die Mehrspannung, die vor allem bei Gasen benötigt wird, um die Elektrolyse ablaufen zu lassen. Die aufzuwendende Spannung ist dabei anders als bei der Elektrolyse von dem Elektrodenmaterial abhängig. PrinzipÜberspannungen treten auf, wenn mindestens ein Teilschritt einer Elektrolysereaktion kinetisch gehemmt d.h. langsamer ist. Bei einer Elektrolysereaktion treten viele Teilschritte auf: 1.) Diffusion der Reaktanden zur Elektrode 2.) Eventuelle Reaktion des Reaktanden vor der Elektrode 3.) Zumindest teilweises Abstreifen der Solvathülle des Reaktanden 4.) Adsorption des Reaktanden 5.) Elektronenübergang vom Reaktanden zur Elektrode (Oxidation des Reaktanden) oder andersherum (Reduktion des Reaktanden) 6.) Desorption des Edukts oder Suchen einer energiearmen Position auf der Oberfläche (bei Abscheidung von Metallen auf demselben Metall) oder Keimbildung (falls sich eine Schicht auf der Elektrode abscheidet) Falls das Edukt desorbiert: 7.) Bildung und/oder Umstrukturierung der Solvathülle, 8.) Eventuelle Reaktion des Edukts vor der Elektrode und 9.) Diffusion des Edukts in die Lösung Überspannungen können bei allen Elektrolysereaktionen auftreten, sie sind allerdings besonders groß bei Gasen. Dabei muss zu den Potentialen der Gase in der Lösung eine fest definierte Überspannung addiert werden, abhängig vom Elektrodenmaterial und vom Gas selbst. Ohne die Überspannung ließe sich die nicht einsetzende Stoffentwicklung bei einer Zersetzungsspannung nicht erklären. Beispiel an einer HCl-ElektrolyseWenn die Überspannung nicht berücksichtigt wird, würde folgende Reaktion ablaufen:
In der Versuchsdurchführung (zum Beispiel mit Graphit-Elektroden) entsteht jedoch Chlor und Wasserstoff. Dies ist mit der Überspannung zu erklären.
|
||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Überspannung_(Elektrochemie) aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. |