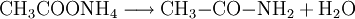Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Ammoniumacetat
Ammoniumacetat, CH3COONH4, ist das Ammonium-Salz der Essigsäure. Es bildet farblose, schwach nach Essigsäure riechende Kristalle, die sich sehr gut in Wasser und gut in Ethanol lösen. Im festen Zustand bildet es eine hygroskopische Masse, die in Lösung neutral reagiert. Produkt-HighlightAmmoniumacetat reizt die Augen, Atmungsorgane und die Haut (Kennzeichnung: Xi). SyntheseAmmoniumacetat lässt sich durch Umsetzung von Ammoniumcarbonat oder Ammoniak mit Eisessig gewinnen. VerwendungVerwendung findet das Ammoniumacetat in der Färberei, bei der Fleischkonservierung und in der biochemischen Laborarbeit. Im Labor wird es zur Herstellung von Pufferlösungen verwendet, wo es den pH-Wert stabilisiert. In der Mikroskopie wird es in Mischung mit Gummi arabicum als Einschlussmittel zur Herstellung von Dauerpräparaten eingesetzt. In der Gentechnik wird die DNA manchmal mit Hilfe von Ammoniumacetat ausgefällt. Im Gegensatz zum Natriumacetat werden so keine Oligonukleotide und keine freien dNTPs mitgefällt, so dass auf diese Art gefällte DNA für die Transfektion von Säugerzellen besser geeignet ist. Sie ist allerdings nicht geeignet, wenn später Kinasen verwendet werden sollen. ReaktionenBeim Erhitzen zerfällt Ammoniumacetat unter Wasserabspaltung zu Acetamid. Kategorien: Reizender Stoff | Acetat | Ammoniumverbindung |
||||||||||||||||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Ammoniumacetat aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. | ||||||||||||||||||||||||||||||||||||||