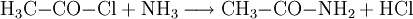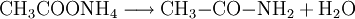Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Acetamid
Produkt-HighlightGewinnung und DarstellungAcetamid wird durch Umsetzung von Acetylchlorid und Ammoniak hergestellt: Es kann ebenfalls durch Erhitzen von Ammoniumacetat erzeugt werden: VerwendungEs dient hauptsächlich als Lösungsmittel, da sich in ihm (im geschmolzenen Zustand) viele Substanzen gut lösen. Außerdem findet es Anwendung in der Herstellung von Methylamin. Biologische BedeutungDie Kristalle sind brennbar. Beim Verbrennen bilden sich toxische Dämpfe (Stickoxide). Der Stoff reagiert mit Säuren und starken Oxidationsmitteln. Der Stoff wird inhalativ aufgenommen und reizt die Haut bzw. Augen. Eine Einwirkung von Acetamid ist an Rötungen und Schmerzen zu erkennen. Bei Tierversuchen traten Geburtsschäden auf und es besteht der Verdacht dass Acetamid beim Menschen Krebserzeugend ist. Kategorien: Gesundheitsschädlicher Stoff | Amid |
||||||||||||||||||||||||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Acetamid aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. | ||||||||||||||||||||||||||||||||||||||||||||||