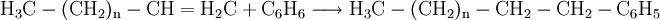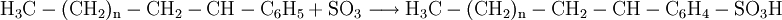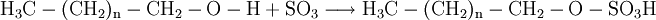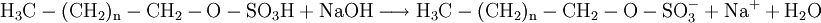Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Anionische TensideAls anionische Tenside bezeichnet man Tenside, die eine negativ geladene funktionelle Gruppe besitzen. Wie alle Tenside sind auch die anionischen Tenside aus einem polaren und einem unpolaren Teil aufgebaut. Als unpolarer Teil dient ein Alkylrest. Die polare, funktionelle Gruppe sind −COO−(Carboxylat), −SO3−(Sulfonat) oder −SO42−(Sulfat). Produkt-Highlight
Typische Vertreter
VerwendungGenerell gilt, dass die anionischen Tenside in Reinigern immer mehr durch die leistungsfähigeren nichtionischen Tenside ersetzt werden. Der Einsatzbereich anionischer Tenside wird sich auf Grund ihrer guten Hautverträglichkeit in Zukunft auf kosmetische Produkte und Handgeschirrspülmittel beschränken. Die Sulfonate ABS und SAS zeigen gute Benetzungseigenschaften und können auch in hartem Wasser eingesetzt werden; sie werden vor allem in pulverförmigen Textilwaschmitteln eingesetzt. Die Seifen sind nur beschränkt einsetzbar, da sie in hartem Wasser unlösliche Kalkseifen bilden und daher unwirksam werden. HerstellungAlkylbenzolsulfonateDas aus der Friedel-Crafts-Alkylierung gewonnene Alkylbenzol wird mit Oleum sulfoniert und mit Lauge neutralisiert. Reaktionen: 1. Addition: Die Addition wird durch H+-Ionen katalysiert. 3. Neutralisation: SeifenDie Seifen gewinnt man direkt aus der basischen Hydrolyse von Fetten und fette Ölen. D. h. die Fette werden mit Basen wie Kalilauge oder Natronlauge zu Seifen umgesetzt (verseift). Mit Natronlauge werden Kernseifen, mit Kalilauge Schmierseifen hergestellt. Reaktion: Früher wurden Seifen aus Tierfetten mit Hilfe von Soda (Na2CO3) oder Pottasche (K2CO3) gewonnen. Reaktion: FettalkoholsulfateFettalkoholsulfate werden durch Umsetzung eines Fettalkohols mit Schwefeltrioxid gewonnen. Reaktion: ÖkologieEinige Tenside werden durch Kleinstlebewesen der Gewässer schlecht abgebaut. Schaumberge bedeckten daher weite Flächen der Gewässer, bis 1964 das Detergentiengesetz nur noch Tenside zuließ, die zu wenigstens 80 % biologisch abbaubar sind. Kategorien: Tensid | Reinigungsmittel |
|
| Dieser Artikel basiert auf dem Artikel Anionische_Tenside aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. |